Самый твердый металл
Самым твердым и при этом легким металлом на нашей планете считается титан. Благодаря своим свойствам, он активно используется в авиации и кораблестроении — материал отлично подходит для изготовления корпусов самолетов и кораблей. К тому же, благодаря прочности и легкости, из титана изготавливают бронежилеты. Этот металл безопасен для человеческого организма, поэтому часто применяется в медицине для изготовления инструментов и даже протезов — искусственных частей тела.

Благодаря выдающимся свойствам, словом «титан» называют видеокарты и прочую электронику, чтобы подчеркнуть их мощность
При нагревании, титан начинает поглощать кислород, хлор, азот и другие газы. Благодаря этому удивительному свойству, металл используется в различных фильтрах — пропуская различные газы через нагретые до 600 градусов Цельсия титановые трубки, можно очистить их от примесей. Таким же образом можно очистить воду от кислорода, что особенно полезно в пищевой промышленности. Считается, что содержащийся в воде кислород ухудшает качество некоторых продуктов — как минимум, он может сократить срок годности пива.
Характеристики самого плотного металла
Ученые сошлись во мнении, что, несмотря на практически одинаковую плотность, иридий совсем чуть-чуть уступает самому тяжелому металлу. Однако полностью физико-химические свойства этих двух элементов пока не изучены.
Редкостью и трудозатратностью добычи обусловлена стоимость осмия – в среднем от $15 000 за грамм. Он внесен в группу платиновых и условно считается благородным, однако название металла противоречит статусу: по-гречески «осме» значит «запах». Из-за высокой химической активности осмий пахнет смесью чеснока или редьки с хлором.
Застывая из расплава, осмий образует красивые кристаллы с интересным сине- или серебристо-голубым отливом. Но, несмотря на красоту, для изготовления драгоценных аксессуаров он не подходит, так как не обладает свойствами, необходимыми ювелирам: ковкостью и пластичностью.
Элемент ценен только из-за особой прочности. Сплавы, в которые добавляют совсем малые дозы самого тяжелого металла, становятся невероятно износостойкими. Обычно им покрывают узлы, подвергающиеся постоянному трению.
История открытия
1803—1804 годы стали для самого тяжелого металла поворотными: именно в это время его открытие проходило практически в условиях соревнований.
Сначала английский химик Смитсон Теннант и его ассистент Уильям Хайд Уолластон, совершившие не одно важное открытие, обнаружили в процессе эксперимента с платиновыми рудами и азотной и соляной кислотами необычный осадок с характерным запахом и поделились своей находкой с другими. Далее эстафету перехватили французские ученые Антуан де Фуркруа и Луи-Николя Воклен и на основе предыдущих и своих собственных исследований заявили об обнаружении нового элемента. Название ему дали «птен», что значит «летучий», так как в результате опытов они получали летучий черный дым
Название ему дали «птен», что значит «летучий», так как в результате опытов они получали летучий черный дым
Далее эстафету перехватили французские ученые Антуан де Фуркруа и Луи-Николя Воклен и на основе предыдущих и своих собственных исследований заявили об обнаружении нового элемента. Название ему дали «птен», что значит «летучий», так как в результате опытов они получали летучий черный дым.
Однако и Теннант не спал: он продолжал свои исследования и не упускал из виду опыты французов. В итоге Смитсон добился более конкретных результатов и в официальном документе, отправленном Лондонскому королевскому обществу, указал, что разделил птен на два родственных элемента: иридий («радуга») и осмий («запах»).
Где применяют
Список сфер применения довольно обширен: авиация, военная и ракетная техника, аэрокосмическая промышленность, медицина. Хотя производители оружия уже задумываются, чем можно заменить самый тяжелый в мире металл, так как осмий слишком трудно обрабатывать.
Почти половина мировых запасов самого тяжелого металла отдана на нужды химической промышленности. Им окрашивают живые ткани под микроскопом, обеспечивая их сохранность. Кроме того, его применяют как краситель при росписи фарфора.
Изотопы самого тяжелого металла используют для изготовления тары для хранения ядерных отходов.
Места природного залегания
В чистом виде осмий обнаружить практически нереально. Обычно этот тяжелый элемент встречается в соединении с иридием. Вещество содержится в месторождениях платиновых руд и на месте падения или в самих попавших на Землю метеоритах.
Вольфрам — самый тугоплавкий металл
› Металлы
01.07.2020
Металл получил название от минерала вольфрамита («Wolf Rahm» с немецкого). Минерал весил немало, и в Швеции горняки назвали его «тунг стен» — тяжелый камень.
Во Франции, США и Великобритании для вольфрама используют название «tungsten».
Как его нашли
История открытия связана со шведским химиком К.В. Шееле. Из неизученного минерала он выделил неизвестную «тунгстеновую» кислоту (WO3·H2O). Братья Элюар выделили из её солей новый элемент. Поскольку работали они с вольфрамитом, то назван был элемент вольфрамом.
Вольфрамовые стержни с кристаллическими наростами
Свойства
Вольфрам относится к переходным металлам. Имеет серебристо-серый цвет. В периодической таблице Менделеева расположен в VI группе и носит атомный № 74.
Физические свойства металла:
- плотность 19,25 г/см3;
- кристаллическая структура объемноцентрированная, кубическая;
- парамагнитен;
- температура плавления 3422 °C;
- цвет искры — желтый, дает пучок коротких прерывистых искр;
- число стабильных изотопов 4.
Некоторые свойства вольфрама уникальны. Тугоплавкость — визитная карточка вольфрама, ею он отличается от других металлов.
| Вольфра́м / Wolframium (W), 74 |
| 183,84(1) а. е. м. (г/моль) |
| 4f14 5d4 6s2 |
| 141 пм |
| 170 пм |
| (+6e) 62 (+4e) 70 пм |
| 2,3 (шкала Полинга) |
| W ← W3+ 0,11 ВW ← W6+ 0,68 В |
| 6, 5, 4, 3, 2, 0 |
| 769,7 (7,98) кДж/моль (эВ) |
| 19,25 г/см³ |
| 3695 K (3422 °C, 6192 °F) |
| 5828 K (5555 °C, 10031 °F) |
| 285,3 кДж/кг52,31 кДж/моль |
| 4482 кДж/кг 824 кДж/моль |
| 24,27 Дж/(K·моль) |
| 9,53 см³/моль |
| кубическаяобъёмноцентрированная |
| 3,160 Å |
| 310 K |
| (300 K) 162,8 Вт/(м·К) |
| 7440-33-7 |
Рекомендуем: ЛАТУНЬ – сплав из легендарной Атлантиды
Месторождения и добыча
Для промышленной добычи пригодны вольфрамиты (гюбнерит, ферберит) и шеелит.
Классификация месторождений:
- штокверковый вольфрамитовый;
- штокверковый шеелитовый;
- жильный вольфрамитовый;
- скарново-шеелитовый.
Крупнейшими запасами вольфрамовых руд обладают:
- Китай;
- Канада;
- Россия;
- Австралия;
- США.
Российские запасы вольфрамовых руд происхождением из коренных месторождений.
Получение
Промышленное получение металла из руды предваряется обогащением. Это дробление, шлифовка, флотация. Затем из концентрата выделяют WO3, который затем восстанавливают до металла водородом при температуре около 700°С.
Компактный вольфрам получают:
- Методом порошковой металлургии. Достоинство метода — возможность равномерного введения присадок.
- Электронно-лучевая плавка, или плавка в электро-дуговых печах. Достоинство метода — возможность получать крупные (до 3 тонн) заготовки металла.
Сплавы
Присадки меняют характеристики полученных сплавов.
| Марка российского сплава | Присадки |
| ВД-20 | 80% вольфрама, 20% меди |
| ВНЖ-95 | 3% никеля, 2% железа |
| ВНМ 2-1 | 2% никеля, 1% меди |
| ВНЖ 7-3 | 7% никеля, 3% железа |
| ВД-30 | 70% вольфрама, 30% меди |
| ВНЖ-97.5 | 1.5% никеля, 1% железа |
Плюсы и минусы металла
| Преимущества | Недостатки |
| Электрическое сопротивление | Высокая плотность |
| Температура плавления | Слабая сопротивляемость окислению |
| Коэффициент линейного расширения | Ломкость при низких температурах |
Цена вопроса
Средняя цена тонны W на конец июня 2020 года составила 24120-24600 долларов США.
Вольфрам — самый тугоплавкий металл Ссылка на основную публикацию
Приложения
Электроника
Танталовый электролитический конденсатор
В основном тантал в виде металлического порошка используется в производстве электронных компонентов, в основном конденсаторов и некоторых мощных резисторов . Танталовые электролитические конденсаторы используют тенденцию тантала к образованию защитного оксидного поверхностного слоя с использованием танталового порошка, спрессованного в форму таблетки, в качестве одной «пластины» конденсатора, оксида в качестве диэлектрика и электролитического раствора или проводящего твердого вещества в качестве другая “тарелка”. Поскольку диэлектрический слой может быть очень тонким (тоньше, чем аналогичный слой, например, в алюминиевом электролитическом конденсаторе), высокая емкость может быть достигнута в небольшом объеме. Из-за преимуществ в размере и весе танталовые конденсаторы привлекательны для портативных телефонов , персональных компьютеров , автомобильной электроники и фотоаппаратов .
Сплавы
Тантал также используется для производства различных сплавов с высокими температурами плавления, прочностью и пластичностью. Легированный другими металлами, он также используется в производстве твердосплавных инструментов для металлообрабатывающего оборудования и в производстве суперсплавов для компонентов реактивных двигателей, химического технологического оборудования, ядерных реакторов , деталей ракет, теплообменников, резервуаров и сосудов. Из-за своей пластичности тантал можно втянуть в тонкую проволоку или нити, которые используются для испарения металлов, таких как алюминий . Поскольку тантал устойчив к воздействию жидкостей организма и не вызывает раздражения, он широко используется при изготовлении хирургических инструментов и имплантатов. Например, пористые танталовые покрытия используются при изготовлении ортопедических имплантатов из-за способности тантала образовывать прямую связь с твердой тканью.
Тантал инертен по отношению к большинству кислот, за исключением плавиковой кислоты и горячей серной кислоты , а горячие щелочные растворы также вызывают коррозию тантала. Это свойство делает его полезным металлом для химических реакционных сосудов и труб для агрессивных жидкостей. Теплообменные змеевики для парового нагрева соляной кислоты изготовлены из тантала. Тантал широко использовался в производстве сверхвысокочастотных электронных ламп для радиопередатчиков. Тантал способен улавливать кислород и азот, образуя нитриды и оксиды, и поэтому помогает поддерживать высокий вакуум, необходимый для трубок, когда они используются для внутренних деталей, таких как решетки и пластины.
Другое использование
Биметаллические монеты отчеканены Банком Казахстана с серебряным кольцом и танталовым центром. В них есть Аполлон-Союз и Международная космическая станция.
Высокая температура плавления и стойкость к окислению позволяют использовать этот металл в производстве деталей вакуумных печей . Тантал чрезвычайно инертен и поэтому образует множество коррозионно-стойких деталей, таких как защитные гильзы , корпуса клапанов и танталовые крепежные детали. Из-за его высокой плотности кумулятивный заряд и гильзы пенетратора, образованные взрывчаткой , были изготовлены из тантала. Тантал значительно увеличивает бронепробиваемость кумулятивного заряда из-за его высокой плотности и высокой температуры плавления. Он также иногда используется в драгоценных часах, например, от Audemars Piguet , FP Journe , Hublot , Montblanc , Omega и Panerai . Тантал также очень биоинертен и используется в качестве материала для ортопедических имплантатов. Высокая жесткость тантала заставляет использовать его в качестве высокопористой пены или каркаса с меньшей жесткостью для имплантатов для замены тазобедренного сустава, чтобы избежать защиты от напряжений . Поскольку тантал является цветным немагнитным металлом, эти имплантаты считаются приемлемыми для пациентов, проходящих процедуры МРТ. Оксид используется для изготовления специальных стекол с высоким показателем преломления для объективов фотоаппаратов .
Области применения
До середины 40-х годов тугоплавкие металлы использовались только как легирующие элементы для улучшения механических характеристик стальных цветных сплавов на основе меди и никеля в электропромышленности. Соединения молибдена и вольфрама применялись также в производстве твердых сплавов.
Техническая революция, связанная с активным развитием авиации, ядерной промышленности и ракетостроения, нашла новые способы использования тугоплавких металлов. Вот неполный перечень новых сфер применения:
- Производство тепловых экранов головного узла и каркасов ракет.
- Конструкционный материал для сверхзвуковых самолётов.
- Ниобий служит материалом сотовой панели космических кораблей. А в ракетостроении его используют в качестве теплообменников.
- Узлы термореактивного и ракетного двигателя: сопла, хвостовые юбки, лопатки турбин, заслонки форсунок.
- Ванадий является основой для изготовления тонкостенных трубок тепловыделяющих элементов термоядерного реактора в ядерной промышленности.
- Вольфрам применяется как нить накаливания электроламп.
- Молибден все шире и шире используется в производстве электродов, применяемых для плавки стекла. Помимо этого, молибден – металл, используемый для производства форм литья под давлением.
- Производство инструмента для горячей обработки деталей.
Рейтинг: /5 – голосов
Применение тугоплавких материалов
Сферы, в которых применяются тугоплавкие металлы и сплавы:
- авиация;
- ракетостроение;
- электроника;
- космический и военный комплекс.
Объединяет все эти сферы использование новейших технологий и процессов. В основном используются в электрических приборах, лампах, электродах, катодах, предохранителях и многом другом.
Нашли они свое применение и в ядерной энергетике. Тугоплавкие металлы применяют для производства труб ядерных реакторов, оболочек и других элементов АЭС.
В химической промышленности нашли свое применение вольфрам, для окраски тканей, и тантал, антикоррозионные свойства которого применяются при изготовлении посуды и аппаратуры.
Использование тугоплавких металлов в составе прокатных сталей усиливает определенные свойства тех. Это способствует увеличению прочности, температуре плавления и многим другим свойствам.
Ежегодно выпускается миллионы тонн тугоплавких металлов по всему миру. Они используются в составе различных сплавов и сталей. Без них невозможно изготовить качественный инструмент и материал. Развитие военно-промышленного комплекса, самолетостроения, кораблестроения, создание космических кораблей, безопасность в атомной промышленности невозможна без их применения.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Путаница с металлами
История металла получилась очень запутанной. Долгое время его принимали за ниобий, и понадобилось больше 30 лет, чтобы доказать обратное. До начала XIX века оба металла не были известны науке. В 1801 году в Южной Америке был найден колумбий. Через год в Швеции и Финляндии Андерс Экеберг обнаружил минерал с частичками неизвестного металла, который назвал танталом в честь мифического персонажа.
В 1809 году Уильям Волластон сравнил два новых для химии вещества. Их свойства были очень похожи, из-за чего учёный заключил, что всё это один и тот же металл. Его выводы подтвердил Фридрих Вёлер, и с тех пор между колумбием и танталом ставили знак равенства.

В середине 40-х годов XIX века Генрих Розе усомнился в утверждениях своих предшественников. Он установил, что тантал и колумбий – отдельные элементы. Чтобы подчеркнуть схожесть металлов, он переименовал колумбий в ниобий в честь легендарной дочери Тантала. Позже выводы Розе неоднократно подтверждались, а ему самому часто приписывается открытие ниобия.
Тантал
Внешне имеет светло-серый цвет с небольшим голубоватым оттенком. Температура плавления близка к 3000 °С. Хорошо поддается основным видам обработки. Его можно ковать, прокатывать, производить волочение для изготовления проволоки. Эти операции не требуют значительного нагрева. Для удобства дальнейшего использования тантал изготавливают в форме фольги и тонких листов. Повышение температуры вызывает активное взаимодействие со всеми газами, кроме инертных – с ними никаких реакций не наблюдается.

Тантал
Из тантала производят внутренние элементы генераторных ламп (магнетронов и клистронов). Он активно используется при производстве пластин в электролитических конденсаторах. Очень удобен для изготовления пленочных резисторов. Активно применяется для изготовления так называемых лодочек в испарителях, в которых осуществляется термическое напыление различных материалов на тонкие пленки.
Ввиду ряда своих уникальных качеств, считается незаменимым в ядерной, аэрокосмической и радиоэлектронной промышленности.
Самый тугоплавкий металл в мире — свойства, получение, применение
Определение «тугоплавкие металлы» не требует дополнительных пояснений в силу исчерпывающей информативности самого термина. Единственным нюансом остается пороговая температура плавления, после которой вещество можно считать тугоплавким.
Где применяется вольфрам?
Широко используют соединения вольфрама. Их применяют в машиностроительной и горнодобывающей промышленностях, для бурения скважин. Из данного металла благодаря его высокой прочности и твердости изготавливают детали двигателей летательных аппаратов, нити накаливания, артиллерийские снаряды, сверхскоростные роторы гироскопов, пули и т.д. Также вольфрам успешно применяется как электрод при аргонно-дуговой сварке. Не обходятся и такие отрасли промышленности без соединений вольфрама – текстильная, лакокрасочная.
Определение
Большинство определений термина тугоплавкие металлы
определяют их как металлы имеющие высокие температуры плавления. По этому определению, необходимо, чтобы металлы имели температуру плавления выше 4,000°F (2,200°C ). Это необходимо для их определения как тугоплавких металлов.
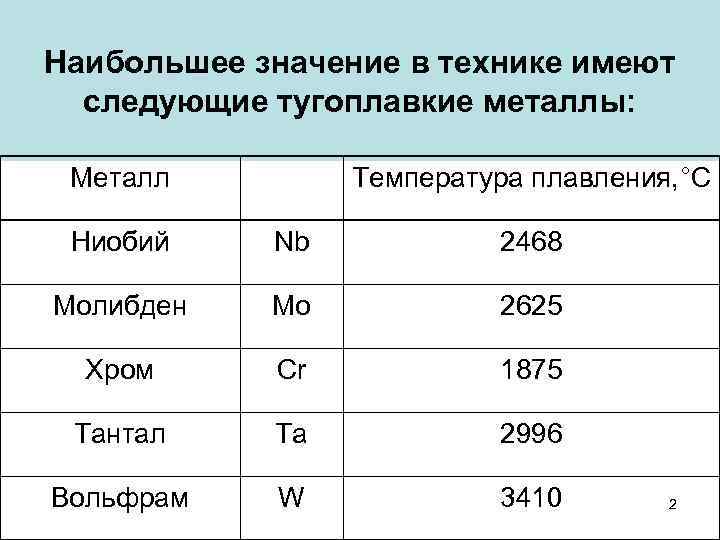
Пять элементов — ниобий, молибден, тантал, вольфрам и рений входят в этот список как основные, в то время как более широкое определение этих металлов позволяет включить в этот список ещё и элементы имеющие температуру плавления 2123 K (1850 °C) — титан, ванадий, хром, цирконий, гафний, рутений и осмий.
Трансурановые элементы (которые находятся за ураном, все изотопы которых нестабильны и на земле их найти очень трудно) никогда не будут относиться к тугоплавким металлам.
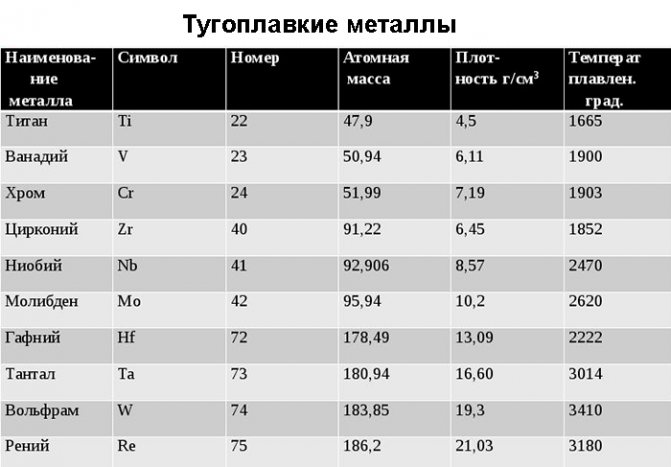
Сравнительная таблица степени тугоплавкости чистых металлов
Следует отметить, что тугоплавкие материалы не ограничиваются исключительно металлами. К этой категории относится ряд соединений – сплавы и легированные металлы, разработанных, чтобы улучшить определенные характеристики исходного материала.
Относительно чистых элементов, можно привести наглядную таблицу степени их температурной устойчивости. Возглавляет ее самый тугоплавкий металл, известный на сегодня, – вольфрам с температурой плавления 3422 0С. Такая осторожная формулировка связана с попытками выделить металлы, обладающие порогом расплава, превосходящим вольфрам.
Поэтому вопрос, какой металл самый тугоплавкий, может в будущем получить совсем иное определение.
Пороговые величины остальных соединений приведены ниже:
- рений 3186;
- осмий 3027;
- тантал 3014;
- молибден 2623;
- ниобий 2477;
- иридий 2446;
- рутений 2334;
- гафний 2233;
- родий 1964;
- ванадий 1910;
- хром 1907;
- цирконий 1855;
- титан 1668.
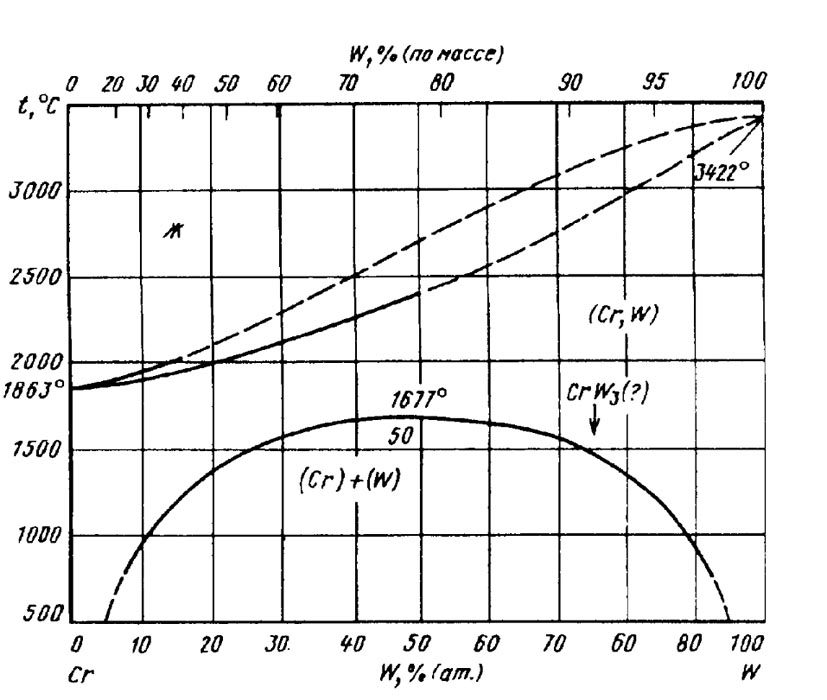
Остается добавить еще один интересный факт, касающийся физических свойств жапропрочных элементов. Температура плавления некоторых из них чувствительная к чистоте материала. Ярким примером этому выступает хром, температура плавления которого может варьироваться от 1513 до 1920 0С, в зависимости от химического состава примесей. Поэтому, данные интернет пространства часто разнятся точными цифрами, однако качественная составляющая от этого не страдает.
Хром в чистом виде
Свойства самых тугоплавких металлов
Так самый тугоплавкий металл в мире (вольфрам) обычно легируется рением, торием, никелем при участии меди и/или железа. Первый делает сплав более коррозионстойким, второй — более надежным, а третий — придает небывалую плотность
Следует обратить внимание, что во всех сплавах вольфрама содержится не более 4/5
Из-за того, что вольфрам одновременно и твердый, и тугоплавкий его обычно применяют в электроснабжении, строении приборов, изготовлении оружия, снарядов, боеголовок и ракет. Более плотные сплавы (на базе никеля) применяют для производства клюшек для игры в гольф. Вольфрам образует и так называемые псевдосплавы. Дело в том, что в них металл не легируется, а наполняется жидким серебром или медью.
За счет разницы в температурах расплава получаются лучшие тепло и электропроводные свойства.
Это дает возможность использовать его для изготовления форм для литья цинковых деталей. Особое направления использования молибдена — в качестве легирующего элемента в стальных сплавах. Сплавы сталь+молибден обладают хорошей износостойкостью и невысокими показателями трения.
Сталь+молибден применяют в для изготовления труб, трубных конструкций, автомобиле и машиностроении.
2.2.5. Сверхпроводящие металлы и сплавы
Сверхпроводимость – это состояние вещества, характеризуемое отсутствием электрического сопротивления. Сверхпроводимость наблюдается у ряда металлов и сплавов при температурах, близких к абсолютному нулю. Температура перехода в сверхпрово-
дящее состояние называется критической температурой сверхпроводимости – Т св .
При температуре ниже Т св электрический ток, наведенный в сверхпроводящем контуре, будет циркулировать бесконечно долго, не убывая, при условии поддержания низкой температуры. Удель-
ное сопротивление материала в сверхпроводящем состоянии составляет порядка 10 -25 Ом·м, что в 10 17 раз меньше, чем у меди.
Физическая природа сверхпроводимости. Впервые явление сверхпроводимости было обнаружено у ртути ( Т св = 4,2 К) голландским физиком Камерлинком-Онессом в 1911 г. Современная теория сверхпроводимости, основанная на квантовых представлениях, была предложена в 1957 г. американскими учеными Бардиным, Купером и Шриффером. Значительный вклад в развитие теории сверхпроводимости внесли работы советского академика Н.Н.Боголюбова.
В металле свободные электроны, движущиеся в среде положительно заряженных ионов, взаимодействуют с тепловыми колебаниями решетки, обмениваясь с ней квантами тепловой энергии – фононами, при этом электроны могут поглощать или отдавать энергию, т.е. изменять свой импульс. Обмен фононами между электронами при участии решетки происходит непрерывно. В результате обменного фононного взаимодействия пара электронов с разными импульсами и антипараллельными спинами испытывают взаимное притяжение и образуют так называемую куперовскую пару .
Рассмотрим упрощенную схему (рис. 9). Электрон 1, движущийся между ионами, притягивает ближайшие ионы, создавая по траектории движения локальную зону повышенной плотности положительного заряда. Электрон 2, движущийся вслед за первым, притягивается этой зоной. В результате, косвенным образом, через решетку, между электронами возникают силы притяжения. Силы притяжения невелики, парные образования слабо локализованы в пространстве, они постоянно распадаются и создаются, образуя электронный конденсат.
При низких температурах ( Т св ) энергия тепловых колебаний решетки чрезвычайно мала и спаренные электроны не рассеиваются на дефектах структуры. Особенность куперовских пар – их импульсная упорядоченность. Электронные волны, описывающие движение пар, имеют одинаковую длину и фазу. Фактически движение всех электронных пар можно рассматривать как распространение одной электронной волны, которая не рассеивается решеткой, «обтекает» дефекты структуры.
Рис. 9. Схема образования электронных пар в сверхпроводнике
При температуре абсолютного нуля все электроны, расположенные вблизи уровня Ферми, связаны в пары. При повышении температуры часть электронных пар распадается. Неспаренные электроны переходят с основных уровней на возбужденные, и их движение затрудняется рассеянием на дефектах структуры. При температуре Т св происходит полный разрыв всех куперовских пар, и состояние сверхпроводимости исчезает.
Сверхпроводники обладают специфическими магнитными свойствами. Поскольку электроны с противоположно направленными спинами связаны в пары, результирующий спиновый момент пары равен нулю, и сверхпроводник становится идеальным диамагнетиком. Как всякие диамагнетики, сверхпроводники выталкиваются из магнитного поля. Внешнее магнитное поле совершенно не проникает в толщину образца, затухая в тончайшем поверхностном слое (10 -7 …10 -8 м). Эффект выталкивания выражен столь сильно, что с помощью магнитного поля можно удерживать постоянный магнит над кольцом из сверхпроводящего материала. Однако состояние сверхпроводимости может быть разрушено, если напряженность магнитного поля превысит некоторое критическое значение Н св .
В настоящее время известно более 30 металлов, обладающих сверхпроводимостью при криогенных температурах, и более 1000
сверхпроводниковых сплавов и химических соединений различных элементов. Параметры некоторых сверхпроводниковых материалов представлены в табл. 5.
Металлы – это самый распространенный материал (наряду с пластмассами и стеклом), который применяется людьми с древних времен. Уже тогда человеку была известна характеристика металлов, он с выгодой использовал все их свойства для создания прекрасных произведений искусства, посуды, предметов быта, сооружений.
Одной из главных черт при рассмотрении этих веществ является их твердость и тугоплавкость. Именно эти качества позволяют определять область использования того или иного металла
Поэтому рассмотрим все физические свойства и особое внимание уделим вопросам плавкости