Общие способы получения металлов

Значительная химическая активность металлов (взаимодействие с кислородом воздуха, другими неметаллами, водой, растворами солей, кислотами) приводит к тому, что в земной коре они встречаются главным образом в виде соединений: оксидов, сульфидов, сульфатов, хлоридов, карбонатов и т. д. В свободном виде встречаются металлы, расположенные в ряду напряжений правее водорода (Аg, Нg, Рt,Аu, Сu), хотя гораздо чаще медь и ртуть в природе можно встретить в виде соединений.
Минералы и черные породы, содержащие металлы и их соединения, из которых выделение чистых металлов технически возможно и экономически целесообразно, называют рудами.
Получение металлов из руд — задача металлургии.
Металлургия — это и наука о промышленных способах получения металлов из руд, и отрасль промышленности.
Любой металлургический процесс — это процесс восстановления ионов металла с помощью различных восстановителей. Суть его можно выразить так:
М n+ + ne−→M
Чтобы реализовать этот процесс, надо учесть активность металла, подобрать восстановитель, рассмотреть технологическую целесообразность, экономические и экологические факторы.
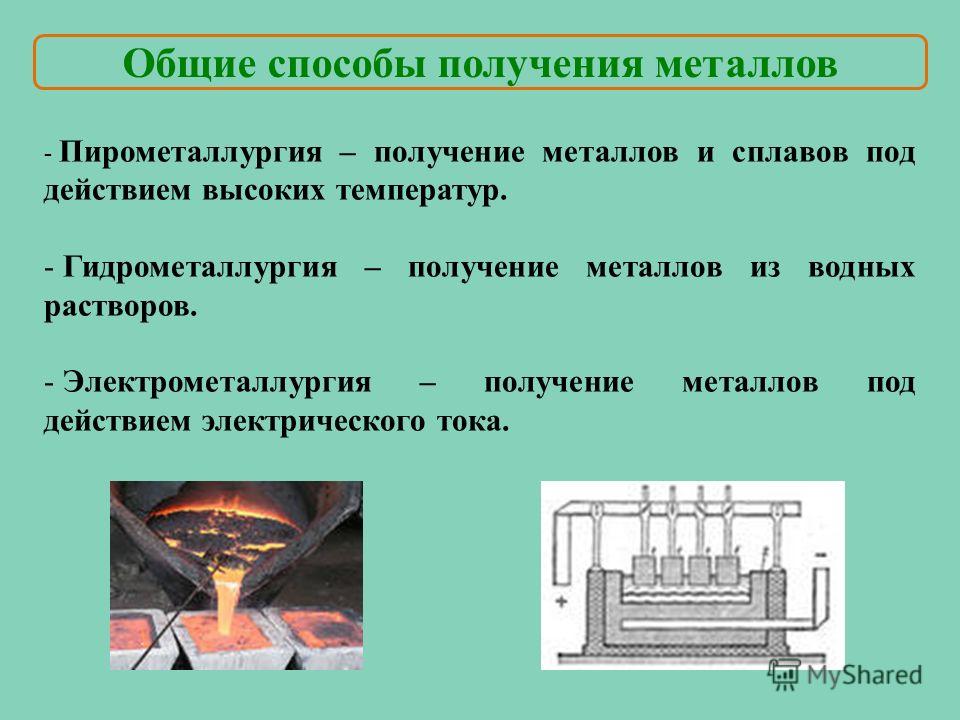
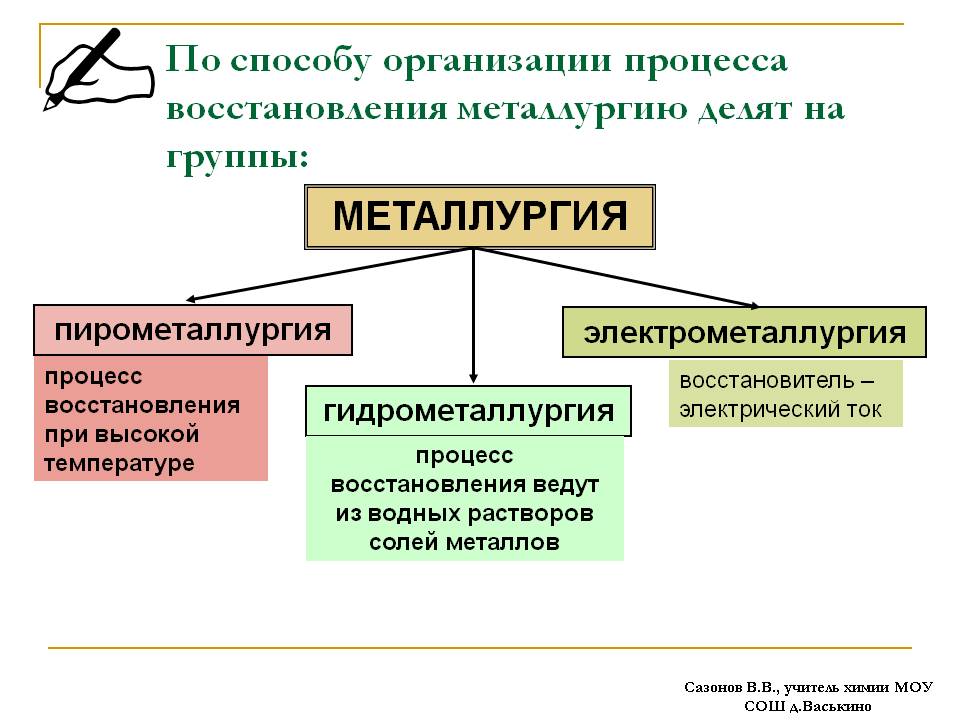
В соответствии с этим существуют следующие способы получения металлов:
• пирометаллургический;
• гидрометаллургический;
• электрометаллургический.
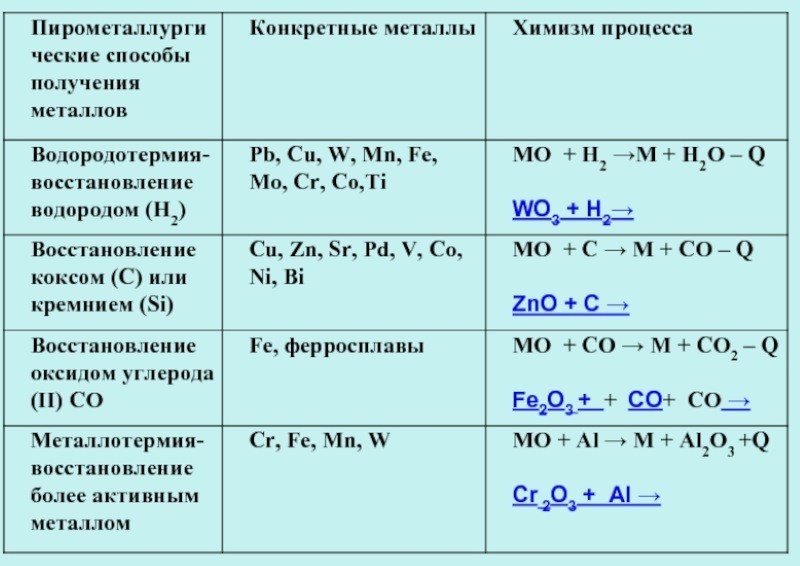
Пирометаллургия
Пирометаллургия — восстановление металлов из руд при высоких температурах с помощью углерода, оксида углерода (II), водорода, металлов — алюминия, магния.
Например, олово восстанавливают из касситерита SnО2, а медь — из куприта Cu2O
прокаливанием с углем (коксом):
Сульфидные руды предварительно подвергают обжигу при доступе воздуха, а затем полученный оксид восстанавливают углем:
Из карбонатных руд металлы выделяют также путем прокаливания с углем, т. к. карбонаты при нагревании разлагаются, превращаясь в оксиды, а последние восстанавливаются углем:
Восстановлением углем можно получить Fе, Сu, Zn, Сd, Ge, Sn, Рb и другие металлы, не образующие прочных карбидов (соединений с углеродом).
В качестве восстановителя можно применять водород или активные металлы:
1) МоO3 + ЗН2 = Мо + ЗН2O (водородотермия)
К достоинствам этого метода относится получение очень чистого металла.
2) TiO2+ 2Мg = Тi + 2МgO (магнийтермия)
ЗМnO2 + 4Аl = ЗМn + 2Аl2O3 (алюминотермия)
Чаще всего в металлотермии используют алюминий, теплота образования оксида
https://youtube.com/watch?v=_-nVROAFWAY
которого очень велика (2А1 + 1,5 O2 = Аl2O3 + 1676 кДж/моль). Электрохимический ряд напряжений металлов нельзя использовать для определения возможности протекания реакций восстановления металлов из их оксидов. Приближенно установить возможность этого процесса можно на основании расчета теплового эффекта реакции (Q), зная значения теплот образования оксидов:
Q= Σ Q1 — Σ Q 2 ,
где Q1— теплота образования продукта, Q2 -теплота образования исходного вещества.
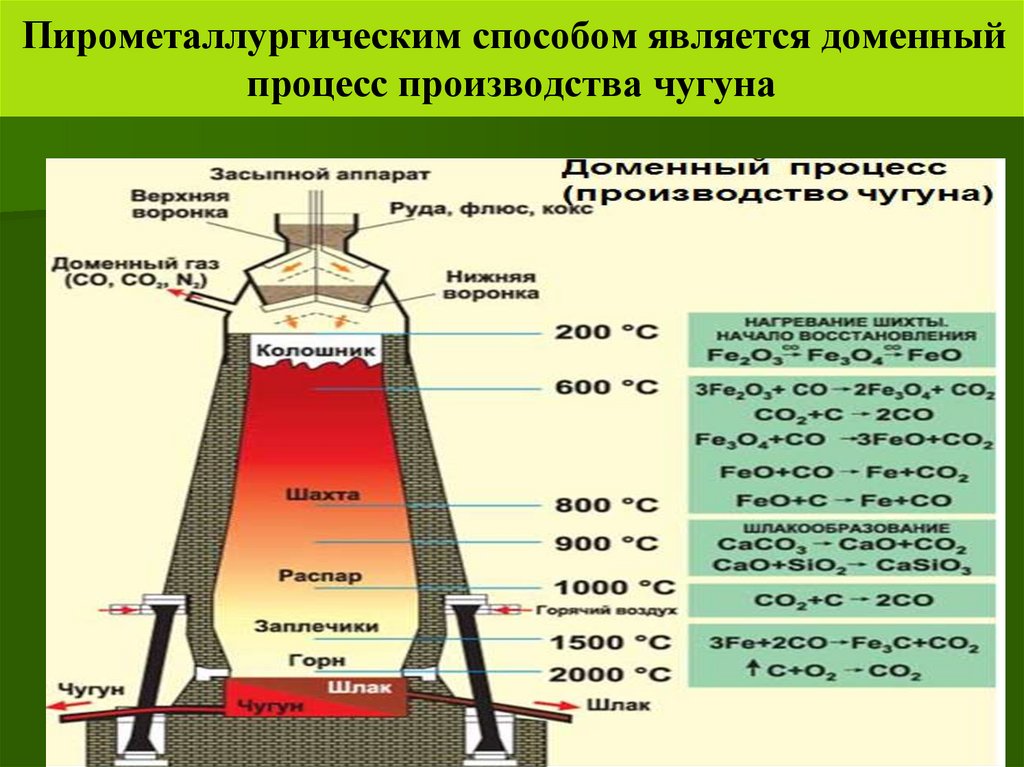
Доменный процесс (производство чугуна):C + O2 = CO2, CO2 + C 2CO3Fe2O3 + CO = 2(Fe2Fe32)O4+ CO2(Fe2Fe32)O4+ CO= 3FeO + CO2FeO + CO= Fe + CO2(чугун содержит до 6,67% углерода в виде зерен графита и цементита Fe3C);
Выплавка стали (0,2-2,06% углерода) проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева.
Продувание воздуха, обогащенного кислородом, приводит к выгоранию из чугуна избыточного углерода, а также серы, фосфора и кремния в виде оксидов.
При этом оксиды либо улавливаются в виде отходящих газов (CO2, SO2), либо связываются в легко отделяемый шлак – смесь Ca3(PO4)2 и CaSiO3. Для получения специальных сталей в печь вводят легирующие добавки других металлов.
Гидрометаллургия
Гидрометаллургия — это восстановление металлов из их солей в растворе.
Процесс проходит в два этапа: 1) природное соединение растворяют в подходящем реагенте для получения раствора соли этого металла; 2) из полученного раствора данный металл вытесняют более активным или восстанавливают электролизом. Например, чтобы получить медь из руды, содержащей оксид меди СuО, ее обрабатывают разбавленной серной кислотой:
СuО + Н2SО4 = СuSO4 + Н2
Затем медь либо извлекают из раствора соли электролизом, либо вытесняют из сульфата железом:
СuSO4. + Fе = Сu + FеSO4
Таким образом, получают серебро, цинк, молибден, золото, уран.
Электрометаллургия
Электрометаллургия — восстановление металлов в процессе электролиза растворов или расплавов их соединений.
Этим методом получают алюминий, щелочные металлы, щелочноземельные металлы. При этом подвергают электролизу расплавы оксидов, гидроксидов или хлоридов.
Примеры:а) NaCl (электролиз расплава) → 2Na + Cl2
Основные процессы
Основным процессом пирометаллургии является рудная плавка, которая проводится при таких высоких температурах, когда продукты химического взаимодействия расплавляются, образуя две жидкие фазы — металлическую или сульфидную и шлаковую. Различают восстановительную и окислительную плавки.
Определяющий процесс восстановительной рудной плавки — это восстановление оксидов металла с получением в конечном итоге расплава металла или его сплава с другими элементами. Типичной восстановительной плавкой является получение чугуна в доменных печах. Восстановительные процессы являются также главными при плавке марганцевых, окисленных никелевых, свинцовых, титановых руд.
Основными реагментами-восстановителями служат углерод, оксид углерода и водород. Оксид углерода образуется в самой печи при неполном горении углерода; основное количество водорода получается в результате разложения вдуваемого в печь природного газа.
Разновидностью восстановительных плавок является металлотермическое получение металлов, при котором в качестве восстановителя какого-то металла (Mn, Cr, V и др.) используется другой металл — с большим сродством к кислороду: Ca; Mg; Al, а также Si. Одним из достоинств металлотермического восстановления является получение металлов, не загрязненных углеродом или водородом.
Типичной окислительном рудной плавкой является переработка в шахтных печах богатых медных сульфидных руд. В ходе плавки окисляется основная доля серы сульфидных минералов, в результате чего выделяется значительное количество тепла. Основным целевым продуктом плавки является расплав сульфидов FeS и Cu2S — штейн.
Чугун и штейн рудных плавок являются, по-существу, полупродуктами, которые требуют дополнительной обработки. Такая обработка заключается в продувке расплавов воздухом или чистым кислородом, в результате чего содержащиеся в сплавах примеси окисляются и переходят либо в шлак (SiO2; MnO; FeO и др.), либо в газ (СО; SO2). Процесс называется конвертированием.
Аналогичным конвертированию является фьюминг-процесс — продувка газом шлаковых расплавов. Отличие его от конвертирования состоит в том, что металлический расплав продувают окислительным газом, а при фьюминговании шлака восстановительным. А во-вторых, продукты окисления металлического расплава — оксиды металлов — образуют вторую жидкую фазу — шлак, а продукты фьюмингования шлака — восстановленные легколетучие металлы (или сульфиды) в парообразном состоянии удаляются из реакционного пространства газовым потоком.
Медь и полезные диеты.

Потребности организма во всех необходимых ему веществах должны восполняться, главным образом, из продуктов в процессе питания. Пища в питательных формах содержит все, что необходимо, включая: витамины, минералы, пищевые волокна и другие природные вещества, оказывающие положительное влияние на здоровье человека.
В некоторых случаях обогащенные продукты питания и пищевые добавки могут быть полезны для обеспечения необходимого количества одного или нескольких питательных веществ.
Диетические рекомендации включают:
Потребление различных овощей и фруктов, цельного зерна, мало жирных или обезжиренных молока и молочных продуктов, а также масла.
Некоторые овощи, фрукты, зерновые и молочные продукты содержат медь.
Употребление разнообразных белковых продуктов, включая морепродукты, постное мясо и птицу, яйца, бобовые, орехи, семена и соевые продукты.
Некоторые мясные продукты, морепродукты, а также орехи и семена богаты медью
Ограничение в рационе насыщенных и трансжиров, добавленных сахаров и соли.
Соблюдение плана по своему ежедневному планы потребления калорий.
, за сегодня 1
Получение меди
После добычи руды возникает следующая проблема: как извлечь из неё необходимый материал? Существует несколько способов.
Одна из древнейших технологий заключалась в сжигании малахитовых руд с ограниченным доступом воздуха. Размещённая в горшках масса, смешанная с углём, сгорала, выделяя при этом угарный газ. Что приводило к достижению желаемого результата – получению достаточно чистой для своего времени меди.
Понятно, что за прошедшие века методы и способы переработки руд претерпевали серьёзные изменения движимые целью достижения наиболее оптимальных результатов при любом виде первичного сырья. Вот почему современная металлургия базируется на трёх основных способах получения меди.
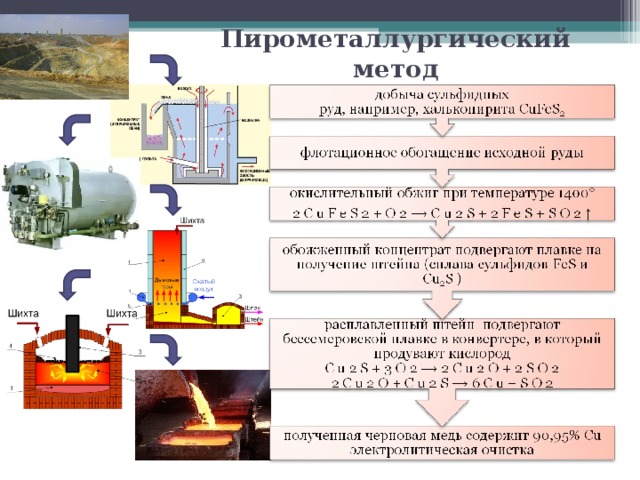
Пирометаллургический метод
Основанный на проведении высокотемпературных процессов, пирометаллургический метод как нельзя лучше подходит для сульфидных руд, подчас достаточно бедных в отношении концентрации меди. Он позволяет извлекать металл даже при содержании его в 0,5%.
Но прежде всего исходное сырьё подвергается обогащению в процессе флотации. Суть его заключается в тщательном измельчении руды, заливке её водой, добавлении туда сложных органических флотореагентов. Они обволакивают частицы минерала, содержащие в своём составе сплавы меди, придавая им несмачиваемость.
На втором этапе этого процесса в растворе создаётся пена, пузырьки которой забирают покрытые органикой частицы. Происходит это под воздействием потока воздуха, в результате чего образования всплывают на поверхность, откуда в дальнейшем забираются. Насыщенная медными соединениями пена собирается, отжимается и высушивается.
После чего полученный концентрат подвергают обжигу при температуре 14000 C. Это необходимо для удаления серы и окисления сульфидов. Затем производят высокотемпературную (14 0000 – 15 0000C) плавку в шахтных печах для получения сплава железа и меди – штейна. Далее в процессе бессемеровской плавки в конвертере под воздействием кислорода получают оксид, а затем и саму черновую медь, содержащую в себе 90,95% металла. При этом сера переходит в кислотный остаток, а железо – в силикатный шлак.
Получить из черновой субстанции чистую медь можно с помощью:
- огневого рафинирования,
- электролиза,
- экзотермической реакции восстановления под воздействием водорода.
Гидрометаллургический метод
Для извлечения меди и ряда других металлов из полиметаллических руд, содержащих в своём составе менее 0,5% искомого минерала, применяют гидрометаллургический метод.
Добытые минералы растворяют с помощью неконцентрированной серной кислоты или аммиака. Из образовавшихся жидкостей в процессе реакции вытеснения получают медь. Для проведения реакции используется металлическое железо.
Электролизный метод
Метод предназначен для получения чистой меди в процессе электролитической реакции.
Его технология заключается в изготовлении чистых медных тонких листовых катодов и толстых пластинчатых анодов из черновой меди. Помещённые затем в ванну, заполненную медным купоросом, они вступают в реакцию под воздействием электрического тока. Происходит растворение меди на анодах и её осаждение на катодах. Освободившиеся примеси удаляют химическими методами.

Медные трубы
Применение железа
Примечательным можно считать тот факт, что из самого Феррума, в его химически чистой форме, в мире практически ничего не делается и не производится. Данный элемент очень легко окисляется, вступая в реакции в кислородом или другими элементами. Так для чего нужна железная руда? Все просто. Феррум, обогащенный карбоном (сплав чугуна) – весьма и весьма популярный материал. Чугун может или служить самостоятельной единицей для изготовления каких-либо вещей и предметов, или же быть промежуточным звеном между железом, и сталью.

Сталь – это сплав железа, углерода и других элементов. Железа должно быть не менее 45%, карбона – от 0,02 до 2,14 процента. Если выше 2,14% – это уже чугун. И уж сталь-то, в десятках своих вариаций, в наше время используется практически везде. Машиностроение, авиация, приборостроение, космические постройки, ядерная энергетика, медицина (существует даже термин – хирургическая сталь), оружейная отрасль (как холодное, так и огнестрельное), сельхозинвентарь, строительная продукция и т.д. За счет такой популярности стали, смело можно утверждать, что ни один металл периодической таблицы не используется так интенсивно и в таких количествах на Земле, как железо.
Действительно, сфер производства продукции железной руды, а также соединений и сплавов на основе Феррума – просто не счесть. Однако, в будущем, при таких темпах и масштабах добычи, перед человечеством могут встать два вопроса: что делать, когда запасы этого металла в недрах нашей планеты станут иссякать? И как поступать с теми гигантскими котлованами по всей планете, которые остаются после проведения добычи железной руды открытым способом?..
Оборудование
Для получения и обработки применяется разное оборудование:
- Для термической обработки — печи, плавильни, горны.
- Для изменения шероховатостей поверхностей — шлифовальные станки, пескоструи.
- Для создания углублений, обработки кромок, торцов — долбежные, сверлильные, фрезеровальные станки.
- Для придания простой или сложной цилиндрической формы — токарные станки.
- Для разрезания заготовок — пилы, лазерные или гидроабразивные резаки.
Современное оборудование оснащается автоматическими системами управления, что ускоряет производство, минимизирует физические затраты со стороны человека.
Самодельный горн (Фото: Instagram / vetal7070)
Производство и потребление металлов
Распространение и сферы применения
Из наиболее ценных и важных для современной техники металлов лишь немногие содержатся в земной коре в больших количествах: алюминий (8,9 %), железо (4,65 %), магний (2,1 %), титан (0,63 %). Природные ресурсы некоторых весьма важных металлов измеряются сотыми и даже тысячными долями процента. Особенно бедна природа благородными и редкими металлами.
Производство и потребление металлов в мире постоянно растёт. За последние 20 лет ежегодное мировое потребление металлов и мировой металлофонд удвоились и составляют, соответственно, около 800 млн тонн и около 8 млрд тонн. Изготовленная с использованием черных и цветных металлов доля продукции в настоящее время составляет 72—74 % валового национального продукта государств. Металлы в XXI веке остаются основными конструкционными материалами, так как по своим свойствам, экономичности производства и потребления не имеют себе равных в большинстве сфер применения.
Из 800 млн т ежегодно потребляемых металлов более 90 % (750 млн т) приходится на сталь, около 3 % (20—22 млн т) на алюминий, 1,5 % (8—10 млн т) — медь, 5—6 млн т — цинк, 4—5 млн т — свинец (остальные — менее 1 млн т). Масштабы производства таких цветных металлов, как алюминий, медь, цинк, свинец, измеряются в млн т/год; таких как магний, титан, никель, кобальт, молибден, вольфрам- в тыс. т, таких как селен, теллур, золото, платина — в тоннах, таких как иридий, осмий и т. п. — в килограммах.
В настоящее время основная масса металлов производится и потребляется в таких странах как США, Япония, Китай, Россия, Германия, Украина, Франция, Италия, Великобритания и другие.
Благодаря своим физическим свойствам (твёрдость, высокая плотность, температура плавления, электропроводность, звукопроводность, внешний вид и другим) они находят применение в различных областях. Применение металлов зависит от их индивидуальных свойств:
- Железо и сталь обладают твердостью и прочностью. Благодаря этим их свойствам они широко используются в строительстве.
- Алюминий ковок, хорошо проводит тепло, обладает высокой прочностью при сверхнизких температурах. Он используется для изготовления кастрюль и фольги, в криогенной технике. Благодаря своей низкой плотности — при изготовлении частей самолётов.
- Медь обладает пластичностью и высокой электропроводностью. Именно поэтому она нашла своё широкое применение в производстве электрических кабелей и энергетическом машиностроении.
- Золото и серебро очень тягучи, вязки и инертны, обладают высокой стоимостью, используются в ювелирном деле. Золото также используется для изготовления неокисляемых электрических соединений.
Сплавы и их применение
В чистом виде металлы применяются незначительно. Гораздо большее применение находят сплавы металлов, так как они обладают особыми индивидуальными свойствами. Наиболее часто используются сплавы алюминия, хрома, меди, железа, магния, никеля, титана и цинка. Много усилий было уделено изучению сплавов железа и углерода. Обычная углеродистая сталь используется для создания дешёвых, высокопрочных изделий, когда вес и коррозия не критичны.
Нержавеющая или оцинкованная сталь используется, когда важно сопротивление коррозии. Алюминиевые и магниевые сплавы используются, когда требуются прочность и легкость.
Медно-никелевые сплавы (такие, как монель-металл) используются в коррозионно-агрессивных средах и для изготовления ненамагничиваемых изделий
Суперсплавы на основе никеля (например, инконель) используются при высоких температурах (турбонагнетатели, теплообменники и т. п.). При очень высоких температурах используются монокристаллические сплавы.
Медно-никелевые сплавы (такие, как монель-металл) используются в коррозионно-агрессивных средах и для изготовления ненамагничиваемых изделий. Суперсплавы на основе никеля (например, инконель) используются при высоких температурах (турбонагнетатели, теплообменники и т. п.). При очень высоких температурах используются монокристаллические сплавы.
Способы получения металлов
В зависимости от того, кокой восстановитель используют в металлургическом процессе различают: пиро – , гидро, электро – и биометаллургию.
Наиболее распространенные способы получения металлов: пирометаллургический и электрометаллургический. Большинство реакций восстановления протекают при высоких температурах (Рис. 2). Так как металлическая связь обладает повышенной прочностью, то выделение металлов в чистом виде из природных соединений проводят при высоких температурах.
Рис. 2. Металлургическое производство
Пирометаллургический способ
Пирометаллургия — получение металлов из руд при высоких температурах при участии восстановителей. В переводе с греческого «пирос» означает «огненный». Используют в качестве восстановителей кокс, диоксид углерода, водород. Применяют активные металлы для получения менее активных.
Пирометаллургия подразделяется на
- карботермия,
- водородотермия,
- металлотермию.
Карботермия: перевод сульфида металла путем обжига в оксид и дальнейшим восстановлением углем до чистого состояния.
2ZnS + 3O2 = 2ZnO + 2 SO2
ZnO + C = CO + Zn
Руды, состоящие из оксидов и сульфидов железа, подвергают карботермии. Проводят восстановление коксом или диоксидом углерода (угарным газом). Получают сплавы железа — чугун и сталь. Первый содержит больше углерода, а также оксидов серы, фосфора и кремния. Углерод снижает твердость и другие характерные для металлов качества.
Химические реакции, лежащие в основе выплавки чугуна:
- C + O2 = CO2↑,
- CO2 + C 2CO↑,
- 3Fe2O3 + CO = 2Fe3O4+ CO2↑,
- Fe3O4 + CO = 3FeO + CO2↑,
- FeO + CO = Fe + CO2↑.
Сталь выплавляют в специальных печах — электрических, конвертерных, мартеновских (Рис. 3). При продувании обогащенного кислородом воздуха выгорает избыточный углерод, его содержание уменьшается до 2% и ниже. Этот способ является более экономически применим, т.к. при помощи него получают сталь и чугун, которые широко используются в современной промышленности.
Рис. 3. Пирометаллургия
Восстановлением углем можно получить железо, медь, цинк, кадмий, германий, олово, свинец и другие металлы. В качестве сырья используют медную (Cu2O), оловянную (SnO2), марганцевую (MnO2) руды.
| Схема получение железа и хрома | (Cr2Fe)O4 + 4C(кокс) = Fe + 2Cr + 4CO↑ |
| Реакция, лежащая в основе выплавки меди | Cu2O + C (кокс) = 2Cu + CO↑ |
| Схема производство олова | SnO2 + 2C (кокс) = Sn + 2CO↑ |
| Процесс выплавки марганца | MnO2 + C(кокс) = Mn + CO2↑ |
| Схема получения свинца | 2PbO + C → Pb + CO↑ |
Металлы можно извлечь из сульфидных руд. Сначала проводят обжиг, затем — восстановление полученного оксида углем. Схемы обжига цинковой обманки и получение цинка:
- 2ZnS +3O2 = 2ZnO + 2SO2↑;
- ZnO + C = Zn + CO↑.
Карбонаты тоже прокаливают с углем для получения оксидов и последующего восстановления углем. Схемы обжига сидерита и восстановления оксида железа:
- FeCO3 = FeO + CO2↑;
- FeO + C = Fe + CO↑.
Водородотермия — производство металлов восстановлением водородом
Достоинством этого металлургического метода является получение очень чистых металлов. Восстановление меди из оксида CuO — пример восстановительных свойств водорода из школьного курса неорганической химии. Схема протекания реакции (Рис 4):
Рис. 4. Восстановление меди водородом
Водородом восстанавливают из оксидов тугоплавкие металлы молибден и вольфрам.
Металлотермия
Проводят восстановление одного металла другим, более химически активным. Этот способ применяют для получения металлов из оксидов и галогенидов.
В зависимости от природы металла-восстановителя различают алюминотермию, или алюмотермию, — восстановление алюминием и магнийтермию — восстановление магнием.
| Схема получение марганца | 3MnO2 + 4Al = 3Mn + 2Al2O3 |
| Процесс выплавки хрома | Cr2O3 + 2Al → 2Cr + Al2O3 |
| Схема получение кальция | 4CaO+ 2Al= 2Ca+ (CaAl2)O4 |
Силикотермия — восстановление металлов кремнием. Процесс протекает согласно схеме: 2MgO + Si → 2Mg + SiO2.
Добыча железных руд в промышленных масштабах
Добывать руду человечество начало очень давно, но чаще всего это было сырье низкого качества со значительными примесями серы (осадочные породы, так называемое «болотное» железо). Масштабы разработки и выплавки постоянно увеличивались. Сегодня выстроена целая классификация различных месторождение железистых руд.
Основные типы промышленных месторождений
Все залежи руды делят на типы зависимо от происхождения породы, что в свою очередь позволяет выделить главные и второстепенные железнорудные районы.
Главные типы промышленных залежей железной руды
К ним относят следующие месторождения:
Залежи различных типов железной руды (железистые кварциты, магнитный железняк), образованной метаморфическим способом, что позволяет добывать на них очень богатые по составу руды. Обычно месторождения связаны с древнейшими процессами образования горных пород земной коры и залегают на образованиях называемых щитами.
Наиболее известные месторождения такого типа: Курская магнитная аномалия, Криворожский бассейн, озеро Верхнее (США/Канада), провинция Хамерсли в Австралии, и железнорудный район Минас-Жерайс в Бразилии.
Залежи пластовых осадочных пород. Эти месторождения образовались вследствие оседания богатых железом соединений, которые имеются в составе разрушенных ветром и водой минералов. Яркий образец железной руды в таких залежах – бурый железняк.
Наиболее известные и большие месторождения — это Лотарингский бассейн во Франции и Керченский на одноименном полуострове (Россия).
- Скарновые месторождения. Обычно руда имеет магматическое и метаморфическое происхождение, пласты которой после образования были смещены в момент образования гор. То есть железная руда, располагающаяся слоями на глубине, была смята в складки и перемещена на поверхность во время движения литосферных плит. Такие залежи размещаются чаще в складчатых областях в виде пластов или столбов неправильной формы. Образовались магматическим способом. Представители таких месторождений: Магнитогорское (Урал, Россия), Сарбайское (Казахстан), Айрон-Спрингс (США) и прочие.
- Титаномагнетитовые залежи руд. Их происхождение магматическое, чаще всего встречаются на выходах древних коренных пород – щитов. К ним относят бассейны и месторождения в Норвегии, Канаде, России (Качканарское, Кусинское).
- В России за 2020 год открыто около сотни месторождений полезных ископаемых
К второстепенным месторождениям относят: апатит-магнетитовые, магно-магнетитовые, сидеритовые, железомарганцевые залежи, разрабатываемые на территории России, стран Европы, Кубы и прочих.
Общая характеристика и способы получения металлов

Значительная химическая активность металлов (взаимодействие с кислородом воздуха, другими неметаллами, водой, растворами солей, кислотами) приводит к тому, что в земной коре они встречаются главным образом в виде соединений: оксидов, сульфидов, сульфатов, хлоридов, карбонатов и т. д. В свободном виде встречаются металлы, расположенные в ряду напряжений правее водорода (Аg, Нg, Рt,Аu, Сu), хотя гораздо чаще медь и ртуть в природе можно встретить в виде соединений.
Минералы и черные породы, содержащие металлы и их соединения, из которых выделение чистых металлов технически возможно и экономически целесообразно, называют рудами.
Получение металлов из руд — задача металлургии.
Металлургия — это и наука о промышленных способах получения металлов из руд, и отрасль промышленности.
Любой металлургический процесс — это процесс восстановления ионов металла с помощью различных восстановителей. Суть его можно выразить так:
М n+ + ne−→M
Чтобы реализовать этот процесс, надо учесть активность металла, подобрать восстановитель, рассмотреть технологическую целесообразность, экономические и экологические факторы.
В соответствии с этим существуют следующие способы получения металлов:
• пирометаллургический;
• гидрометаллургический;
• электрометаллургический.
Пирометаллургия
Пирометаллургия — восстановление металлов из руд при высоких температурах с помощью углерода, оксида углерода (II), водорода, металлов — алюминия, магния.
Например, олово восстанавливают из касситерита SnО2, а медь — из куприта Cu2O
прокаливанием с углем (коксом):
Сульфидные руды предварительно подвергают обжигу при доступе воздуха, а затем полученный оксид восстанавливают углем:
Из карбонатных руд металлы выделяют также путем прокаливания с углем, т. к. карбонаты при нагревании разлагаются, превращаясь в оксиды, а последние восстанавливаются углем:
В качестве восстановителя можно применять водород или активные металлы:
1) МоO3 + ЗН2 = Мо + ЗН2O (водородотермия)
К достоинствам этого метода относится получение очень чистого металла.
2) TiO2+ 2Мg = Тi + 2МgO (магнийтермия)
ЗМnO2 + 4Аl = ЗМn + 2Аl2O3 (алюминотермия)
Чаще всего в металлотермии используют алюминий, теплота образования оксида
которого очень велика (2А1 + 1,5 O2 = Аl2O3 + 1676 кДж/моль). Электрохимический ряд напряжений металлов нельзя использовать для определения возможности протекания реакций восстановления металлов из их оксидов. Приближенно установить возможность этого процесса можно на основании расчета теплового эффекта реакции (Q), зная значения теплот образования оксидов:
Q= Σ Q1 — Σ Q 2 ,
где Q1— теплота образования продукта, Q2 -теплота образования исходного вещества.
Доменный процесс (производство чугуна):C + O2 = CO2, CO2 + C 2CO3Fe2O3 + CO = 2(Fe2Fe32)O4+ CO2(Fe2Fe32)O4+ CO= 3FeO + CO2FeO + CO= Fe + CO2(чугун содержит до 6,67% углерода в виде зерен графита и цементита Fe3C);
Выплавка стали (0,2-2,06% углерода) проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева.
Продувание воздуха, обогащенного кислородом, приводит к выгоранию из чугуна избыточного углерода, а также серы, фосфора и кремния в виде оксидов.
При этом оксиды либо улавливаются в виде отходящих газов (CO2, SO2), либо связываются в легко отделяемый шлак – смесь Ca3(PO4)2 и CaSiO3. Для получения специальных сталей в печь вводят легирующие добавки других металлов.
Гидрометаллургия
Гидрометаллургия — это восстановление металлов из их солей в растворе.
Процесс проходит в два этапа: 1) природное соединение растворяют в подходящем реагенте для получения раствора соли этого металла; 2) из полученного раствора данный металл вытесняют более активным или восстанавливают электролизом. Например, чтобы получить медь из руды, содержащей оксид меди СuО, ее обрабатывают разбавленной серной кислотой:
СuО + Н2SО4 = СuSO4 + Н2
Затем медь либо извлекают из раствора соли электролизом, либо вытесняют из сульфата железом:
СuSO4. + Fе = Сu + FеSO4
Таким образом, получают серебро, цинк, молибден, золото, уран.
Электрометаллургия
Электрометаллургия — восстановление металлов в процессе электролиза растворов или расплавов их соединений.
Этим методом получают алюминий, щелочные металлы, щелочноземельные металлы. При этом подвергают электролизу расплавы оксидов, гидроксидов или хлоридов.
Примеры:а) NaCl (электролиз расплава) → 2Na + Cl2