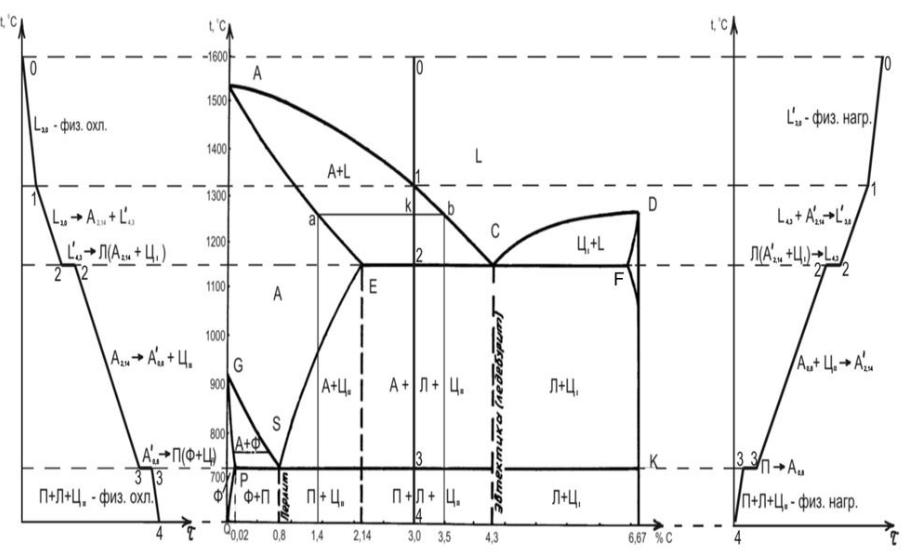
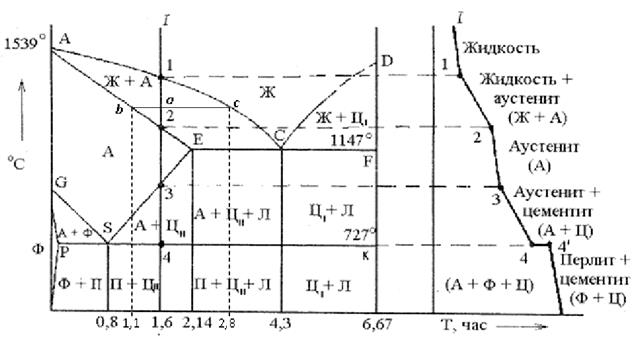
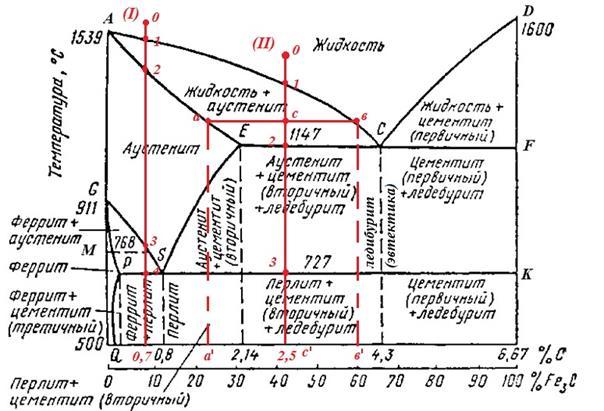
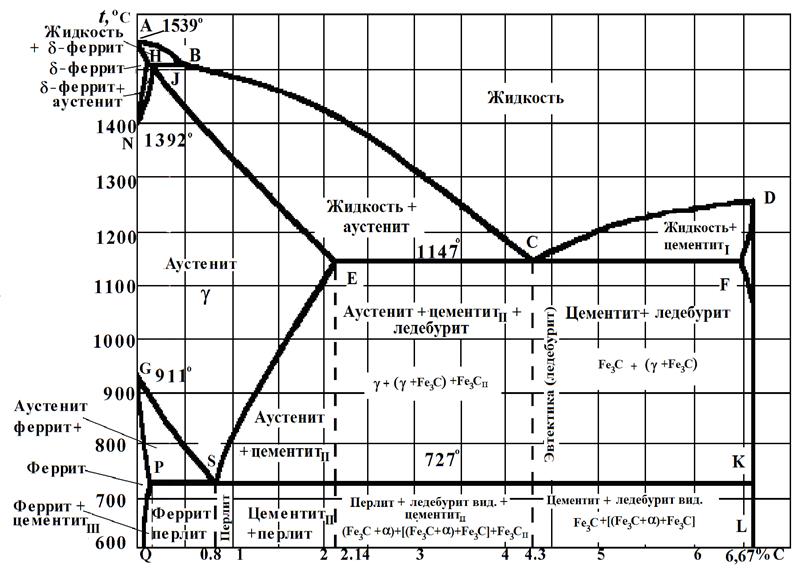
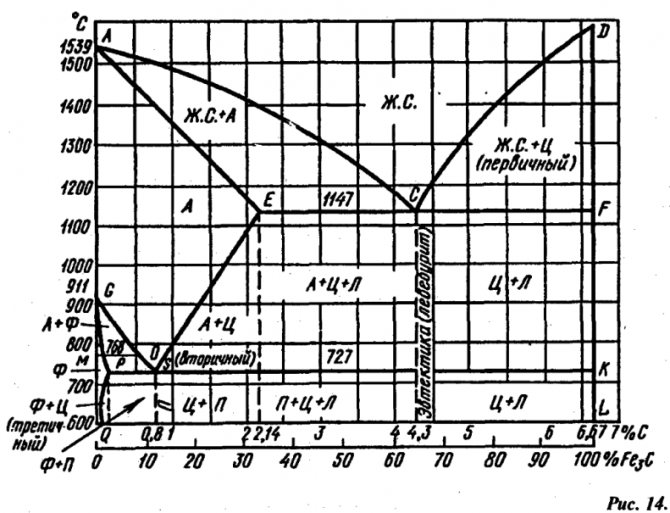
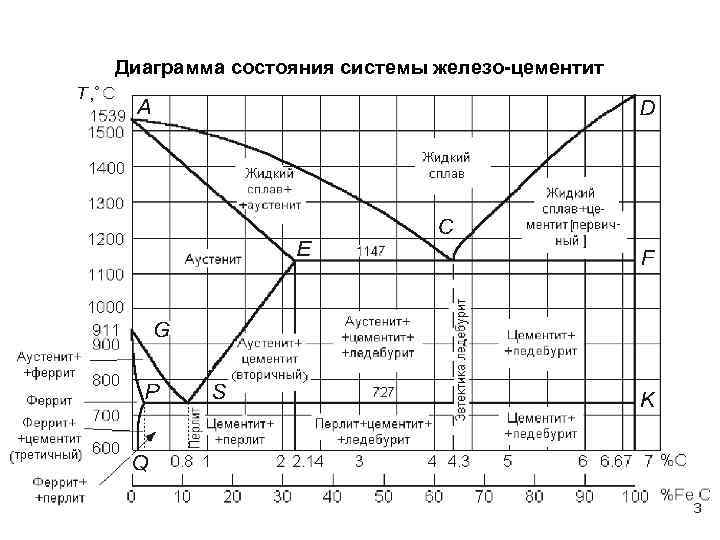
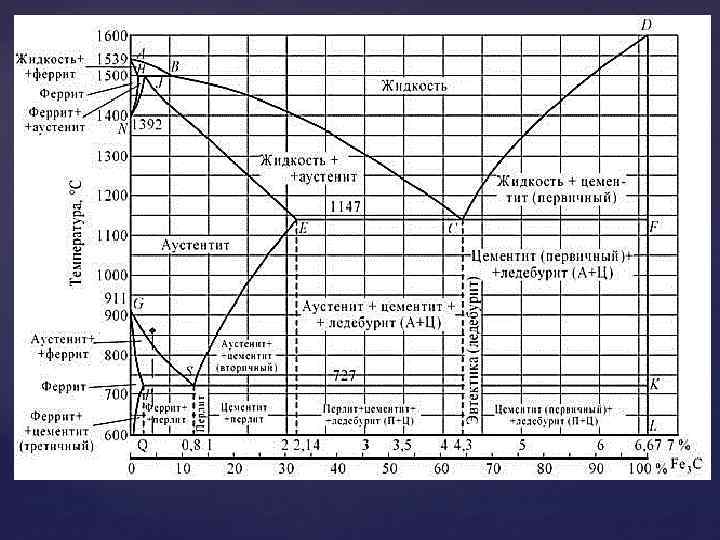
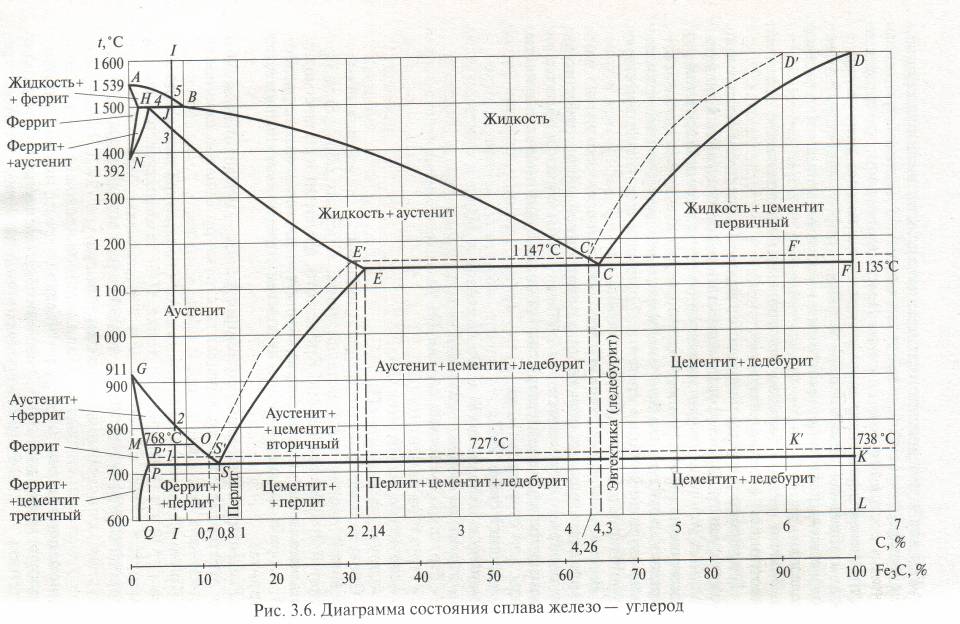
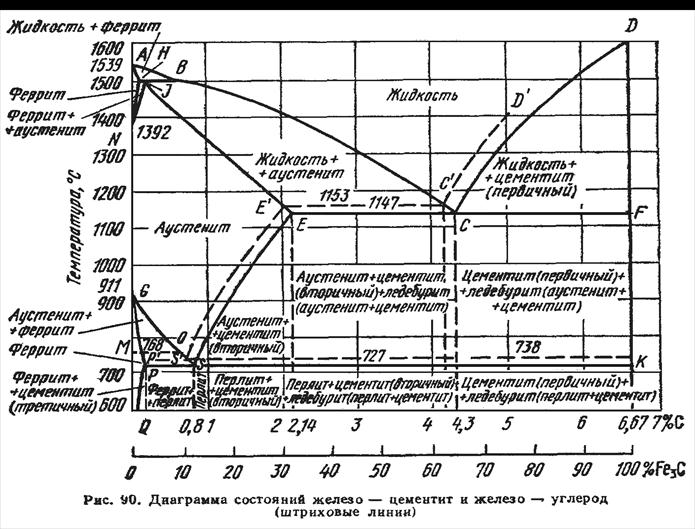
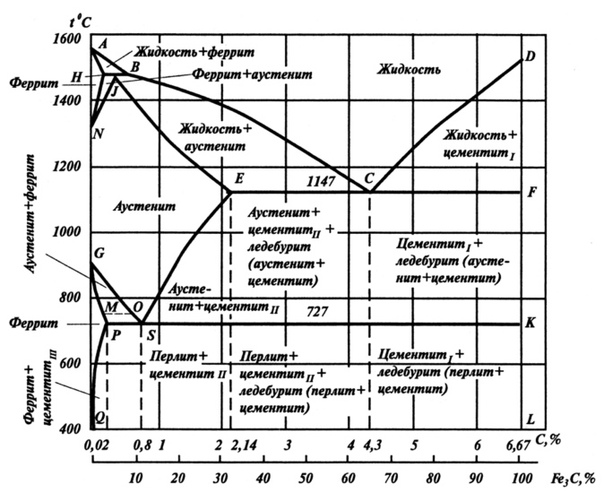
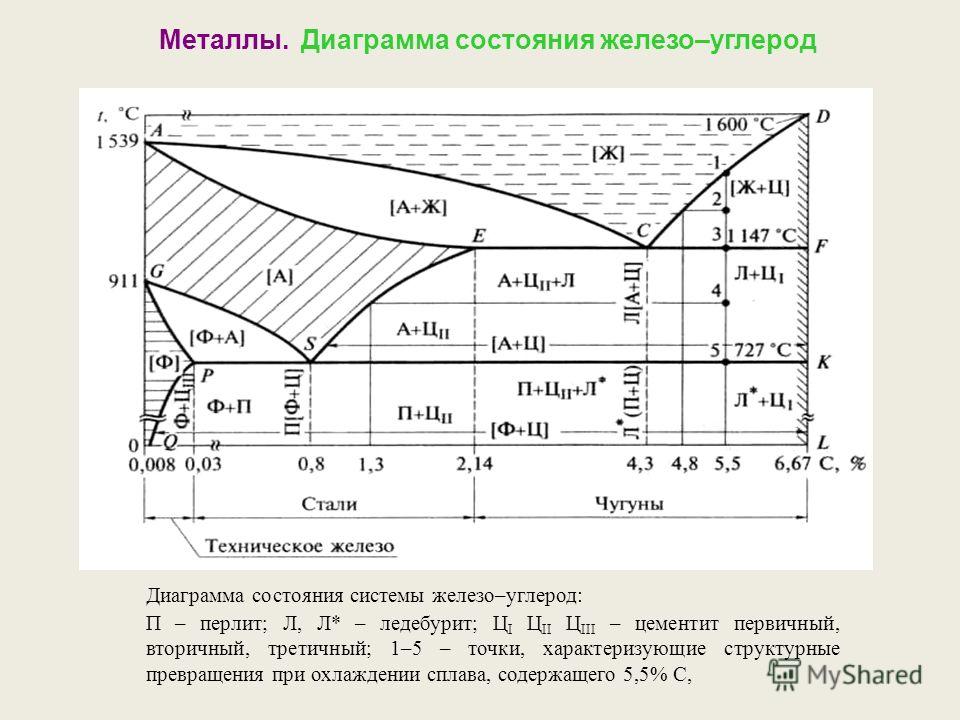
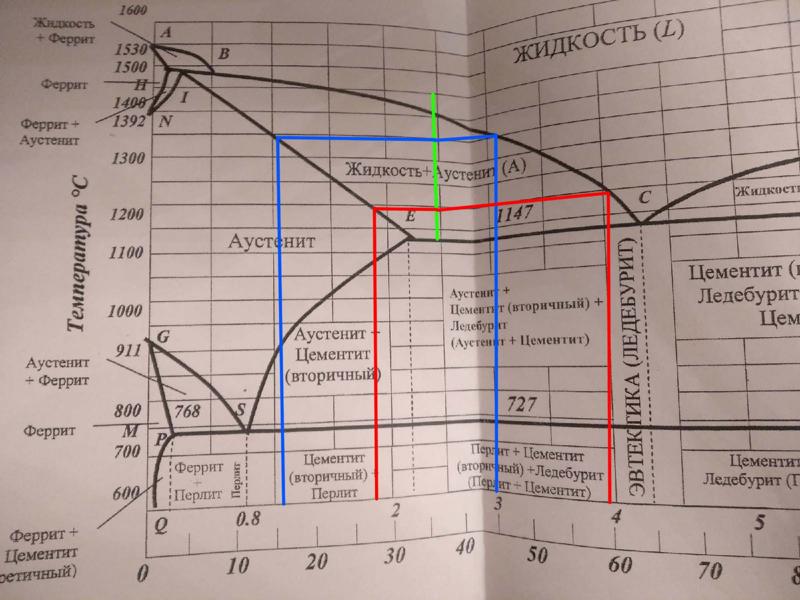
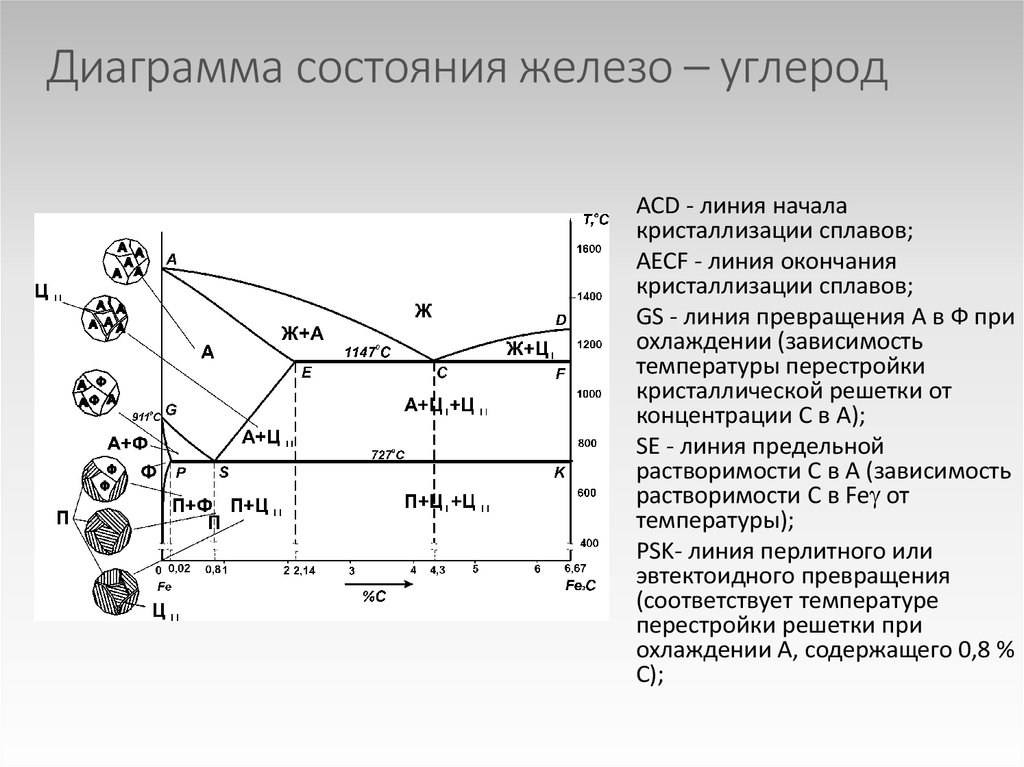
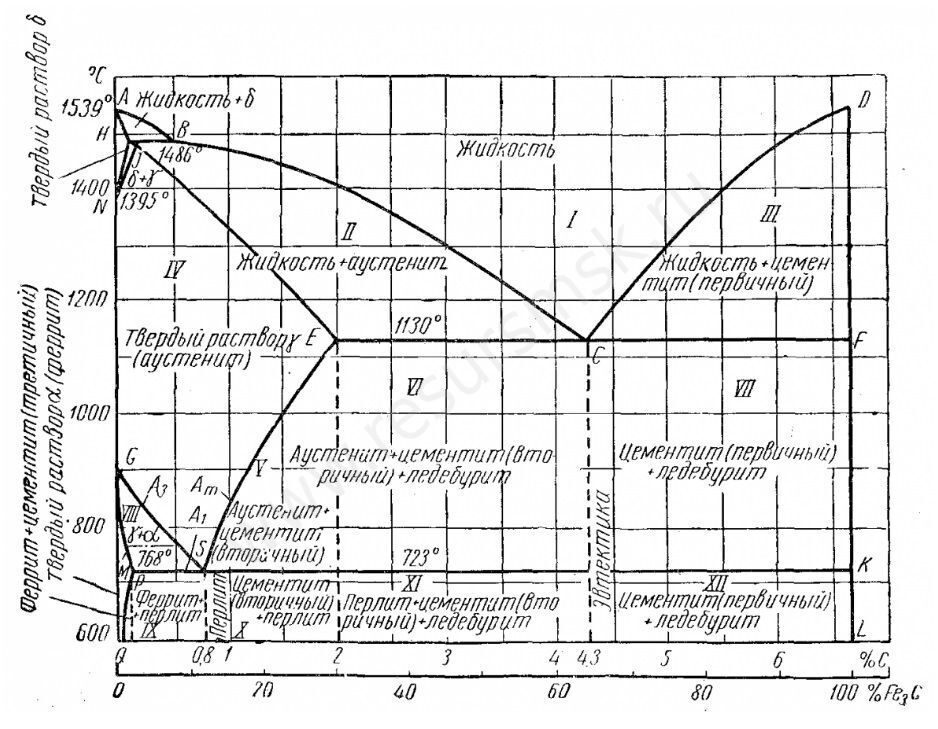
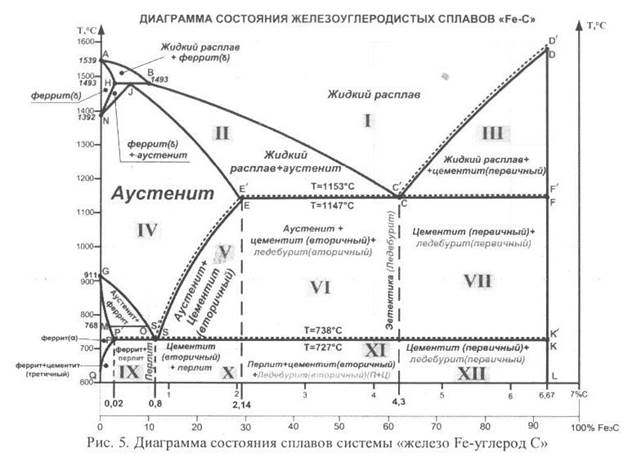
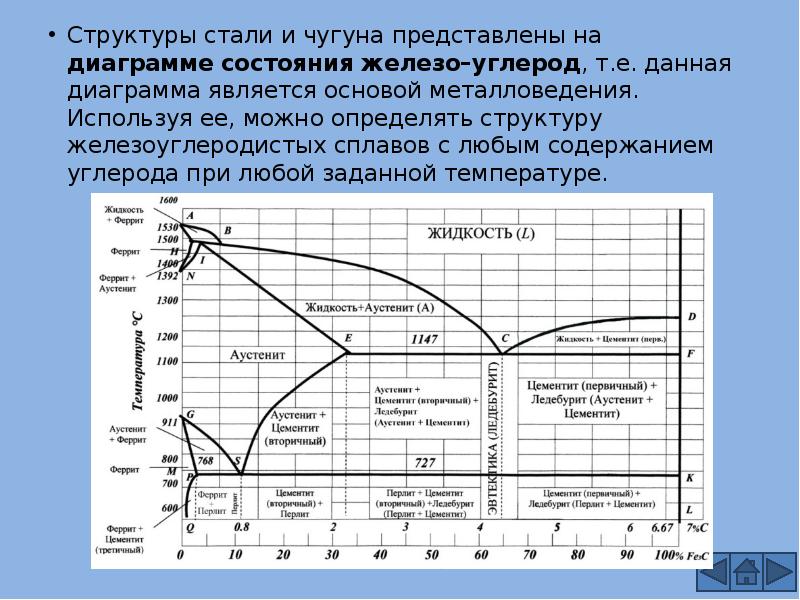
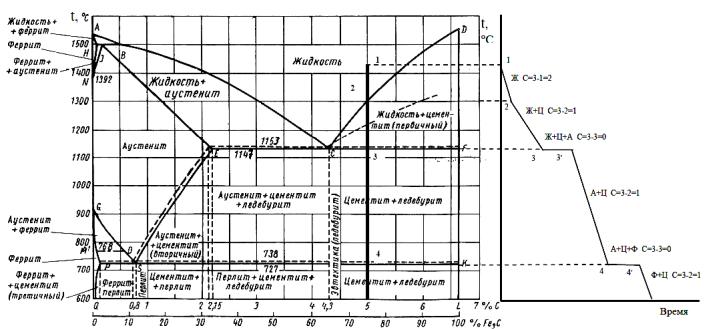
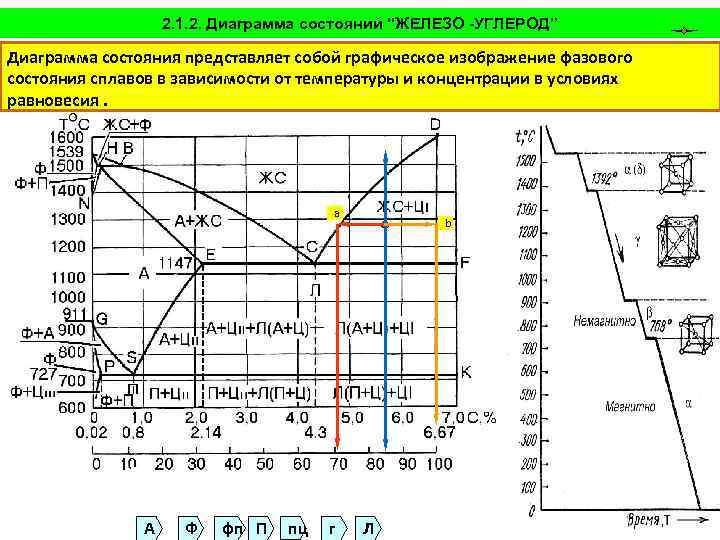
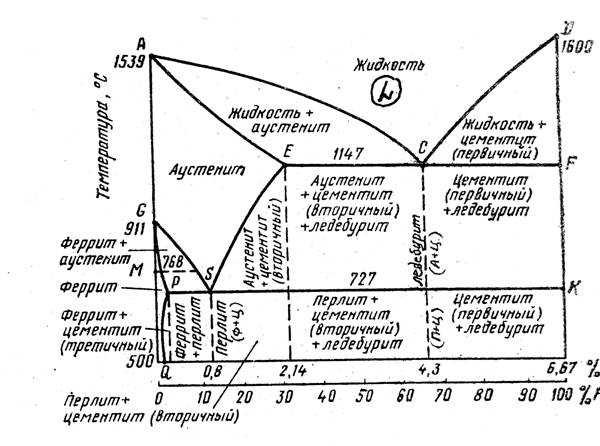
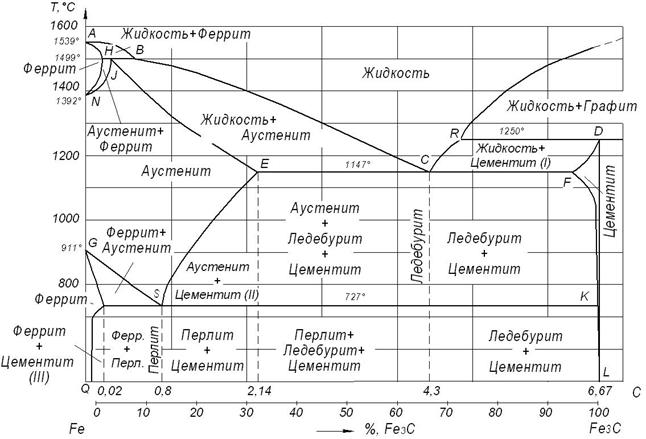
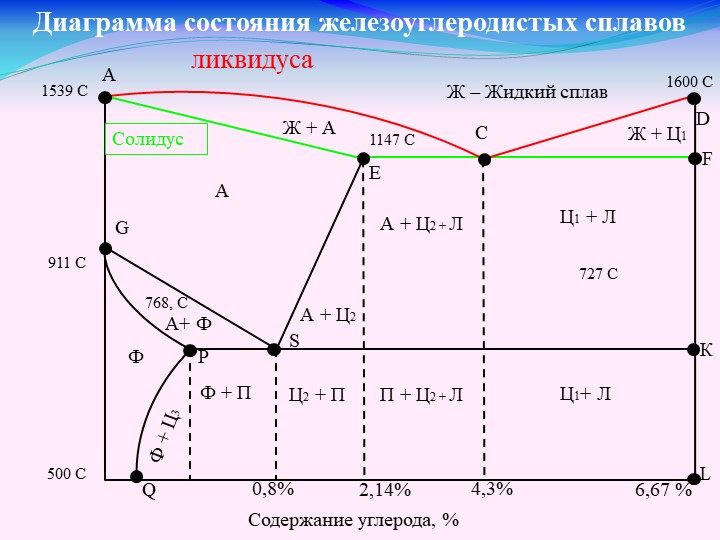
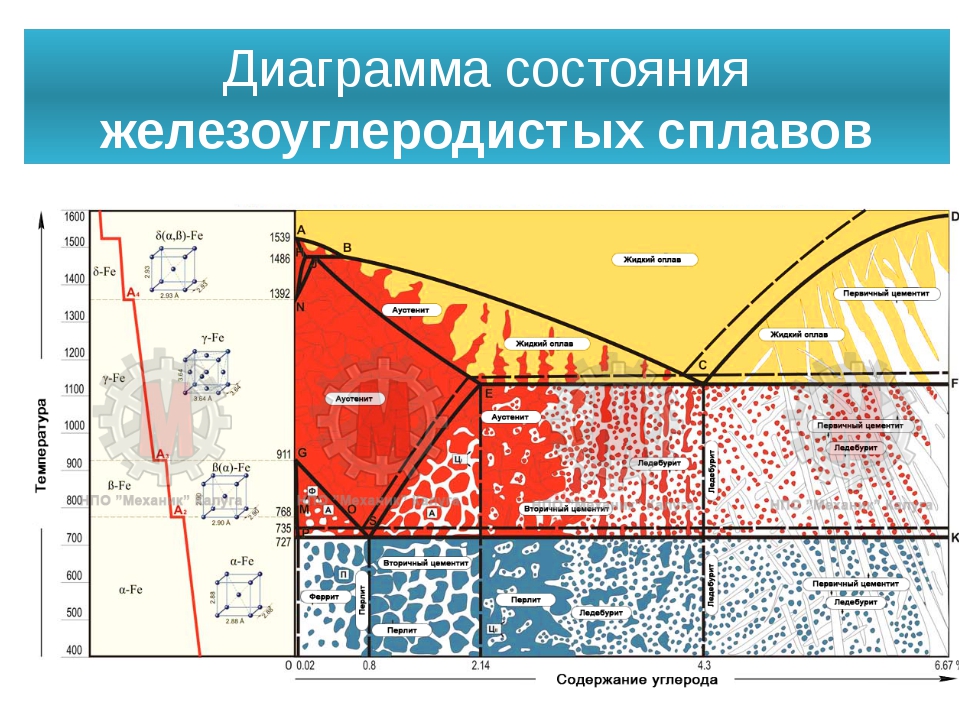
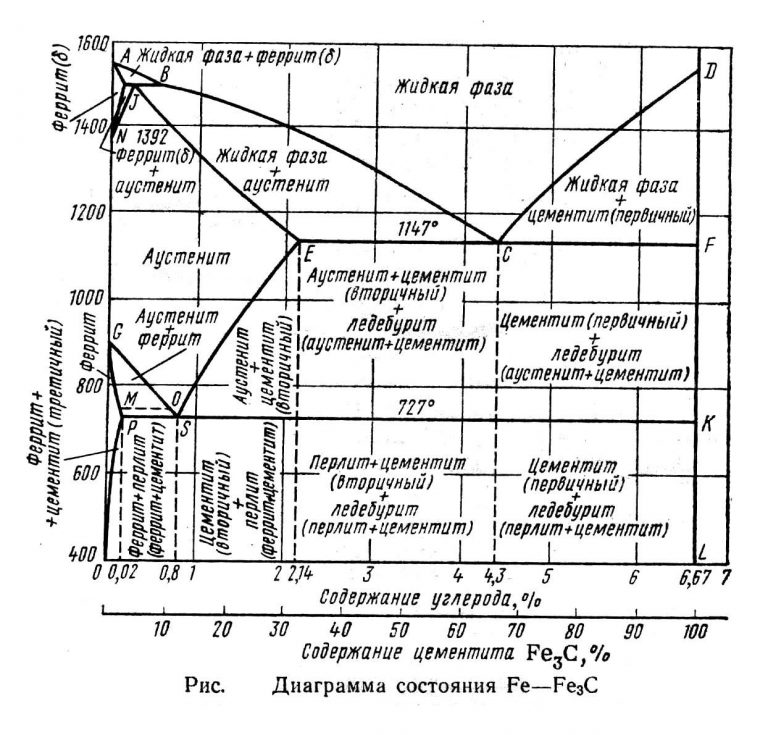
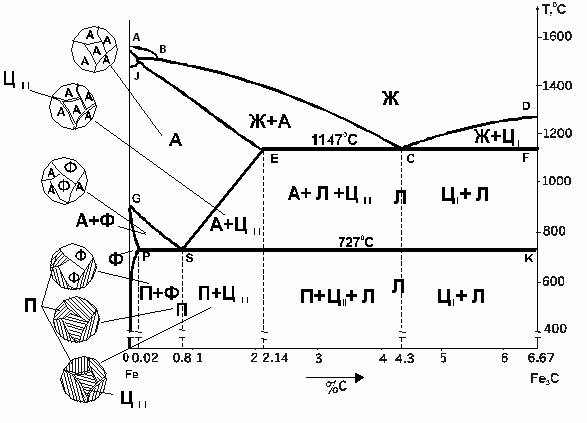
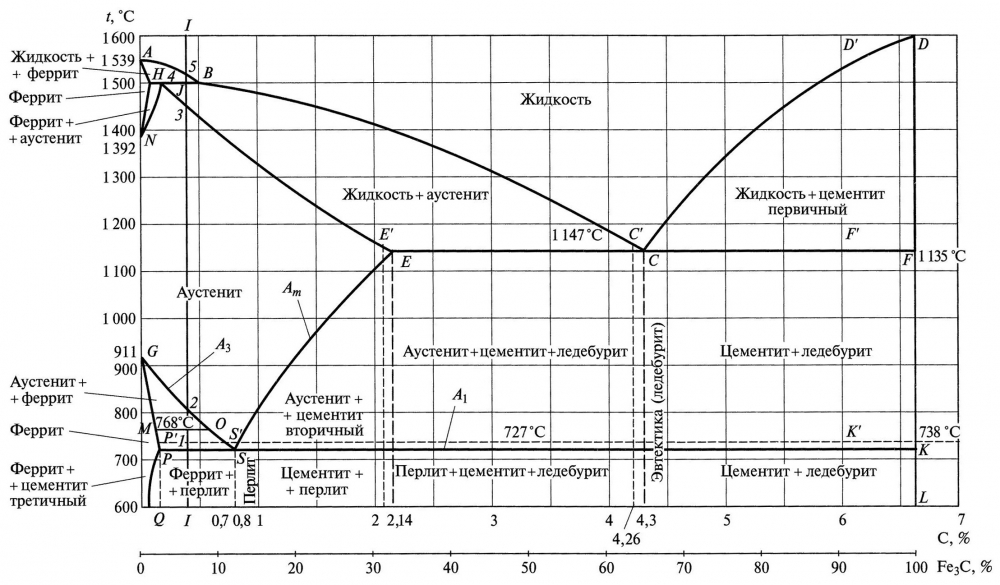
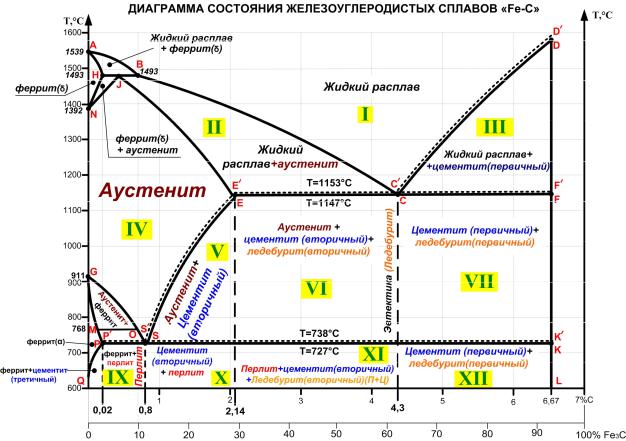
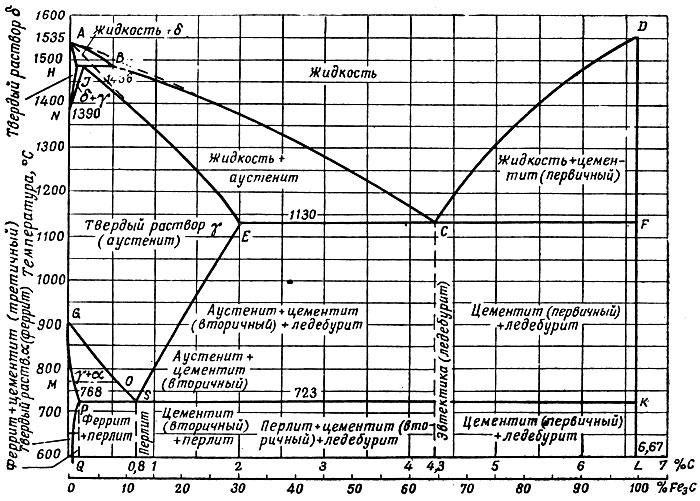
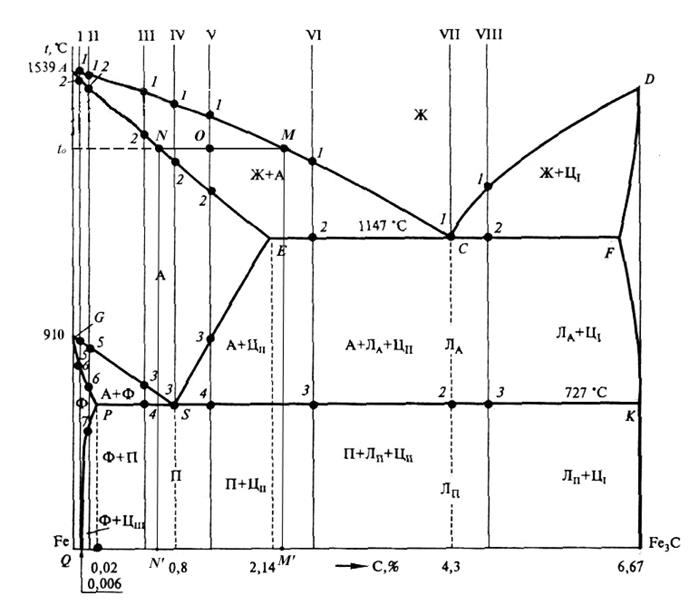
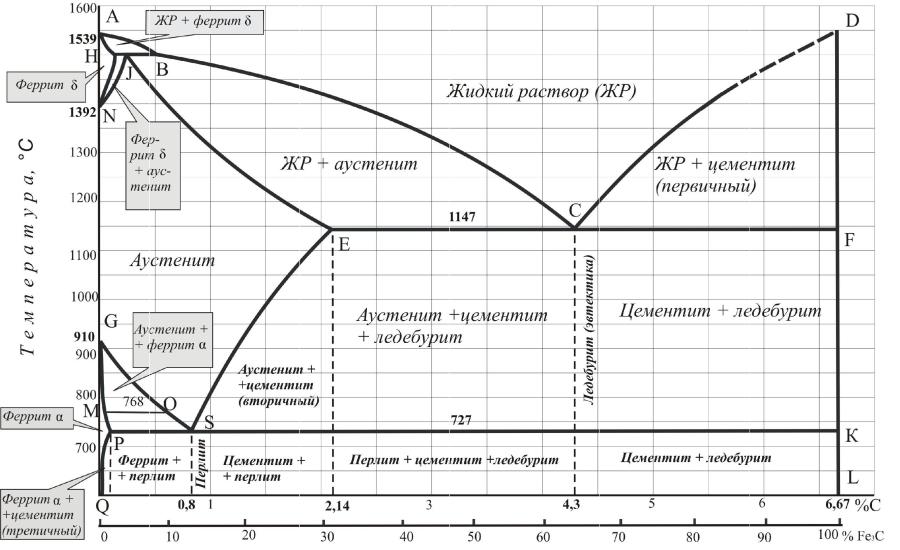
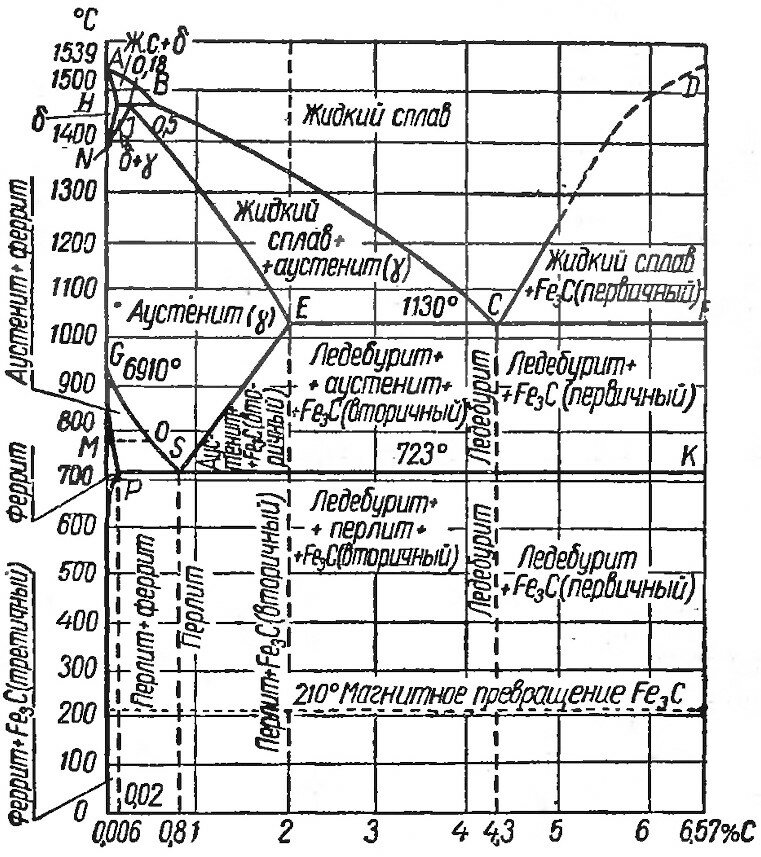
Основные линии диаграммы железо-цементит
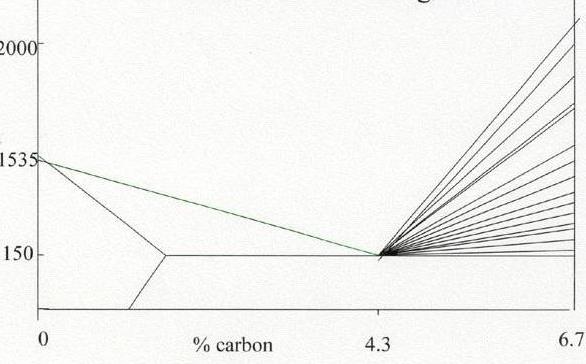
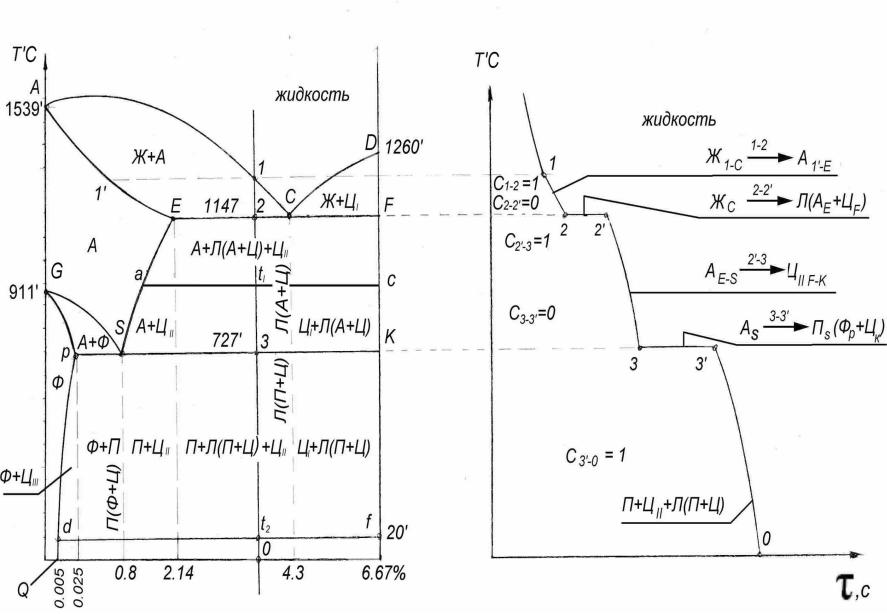
Линия ABCD – это линия ликвидус. Она говорит о том, что любой сплав при температурах, лежащих выше этой линии, находится полностью в жидком состоянии. При пересечении сплавом этой линии в процессе нагревания здесь заканчивается процесс плавления, а при пересечении этой линии в процессе охлаждения здесь будет начинаться процесс кристаллизации.
Линия AHJECF – это линия солидус. Она говорит о том, что любой сплав при температурах, лежащих ниже этой линии, находится полностью в твердом состоянии. При пересечении сплавом этой линии в процессе охлаждения здесь заканчивается процесс кристаллизации, а при пересечении этой линии в процессе нагревания здесь будет начинаться процесс плавления.
Линия HJB– это граница перитектической реакции. На этой линии при постоянной температуре 1499 °С идет перитектическое превращение, заключающееся в том, что жидкая фаза (Ж) реагирует с ранее образовавшимися кристаллами феррита (δ), в результате чего образуется аустенит (А): .
Линия ECF– это граница эвтектической реакции. На этом участке при постоянной температуре 1147 °С идет эвтектическое превращение, заключающееся в том, что жидкость, содержащая 4,3 % углерода превращается в эвтектическую смесь аустенита и цементита: .
Эвтектика системы железо – цементит называется ледебуритом (Л), по имени немецкого ученого А. Ледебура, содержит 4,3 % углерода.
Линия PSK – это граница эвтектоидной реакции. По линии PSK при постоянной температуре 727 °С идет эвтектоидное превращение, заключающееся в том, что аустенит, содержащий 0,8 % углерода, превращается в эвтектоидную смесь феррита и цементита: .
По механизму данное превращение похоже на эвтектическое, но протекает в твердом состоянии.
Эвтектоид системы железо – цементит называется перлитом (П), содержит 0,8% углерода. Название получил за то, что на полированном и протравленном шлифе наблюдается перламутровый блеск.
Перлит может существовать в зернистой и пластинчатой форме, в зависимости от условий образования.
Линия AHN –
это граница предельной растворимости углерода в δ-железе. Твердый раствор углерода в δ-железе получил название высокотемпературного феррита. На отечественных диаграммах он чаще всего обозначается греческой буквой δ.
Линия NJESG– это граница предельной растворимости углерода в γ-железе. Твердый раствор углерода в γ-железе получил название аустенита. На отечественных диаграммах он обычно обозначается прописной буквой А.
Линия QPG– это граница предельной растворимости углерода в α-железе. Твердый раствор углерода в α-железе получил название феррита. На отечественных диаграммах чаще всего он обозначается прописной буквой Ф.
Линия ES– граница перенасыщения аустенита углеродом. При пересечении сплавом этой линии в процессе охлаждения на ней выделяется вторичный цементит, а в процессе нагревания – исчезает вторичный цементит.
Линия PQ– это граница перенасыщения углеродом феррита. При пересечении сплавом этой линии в процессе охлаждения из феррита будет выделяться третичный цементит, а в процессе нагревания – будет исчезать третичный цементит.
Строение и свойства
При повышении температуры аустенитные стали превращаются в жидкий раствор с определённым процентным отношением железа и углерода. Если температура раствора превышает линию так называемого ликвидуса (это около 1700 °C),образовавшийся расплав становится статически неустойчивым. Его состояние оценивают по двум составляющим:фазовой и структурной.
Для первой составляющей основным показателем является фаза состояния полученной смеси. Она определяет состояние металла по следующим показателям:
- раствора углерода в железе;
- количество различных образований (непосредственно феррит, в том числе высокотемпературный, аустенит, цементит).

Структурная составляющая часть образца определяется как гомогенная или квазигомогенная форма. Общая структура образовавшегося феррита составляет равноосные кристаллы. В трёхмерном пространстве решётка ферритной фазы представляет объёмно-центрированный куба. Эти кристаллы определяют твёрдость феррита и способность углерода в нём растворяться. Опыт показывает, что при температуре равной 727 градусов в феррите растворяется только 0,02% углерода.
Кроме этого к основным свойствам феррита относятся:
- обладает сильными ферромагнитными свойствами (до температуры 770 °С — точка Кюри);
- является теплопроводным элементом;
- хорошим проводником электрического тока;
- обладает повышенной пластичностью.
К основным недостаткам относятся невысокая прочность и недостаточная твёрдость. Последний показатель зависит от величины образованного зерна и находится в интервале от 65 до 130 НВ.
В зависимости от этапа проходящих превращений ферритная фаза находится в следующих состояниях:
- как основа кристаллической решётки образовавшегося сплава;
- второе или избыточное состояние (располагается по границам так называемых перлитных образований);
- элемент феррито-графитного эвтектоида.
Каждое состояние требует точного определения и выявления возникающих преобразований. От них во многом зависят характеристики конечного продукта.Полное отсутствие ферритного образования или незначительное его содержание проявляется с образованием горячих трещин. Завышенное содержание этого показателя снижает пластичность, ударную вязкость и антикоррозийную стойкость.
Чтение диаграммы железо-углерод
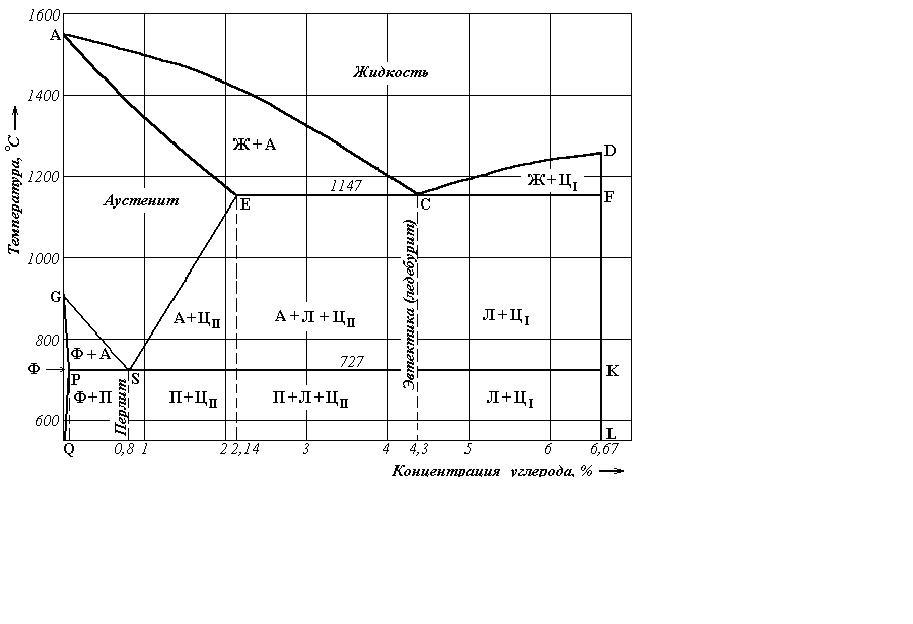
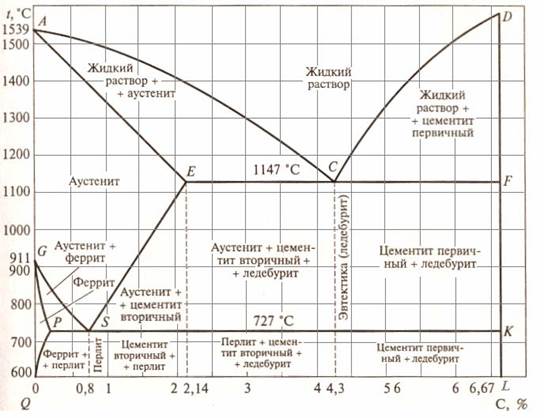
Состав сплава с данным исходным содержанием углерода при заданной температуре мы можем увидеть, двигаясь по вертикальной линии, соответствующей содержанию углерода в сплаве.
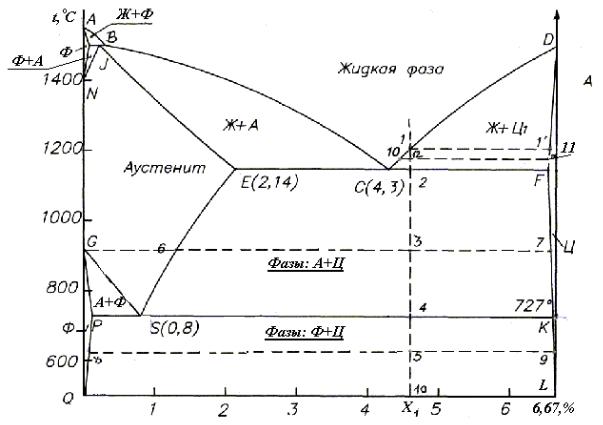
Рассмотрим, например, область AEC. С ней соседствуют области аустенита AESG и жидкой фазы. Сплавы в ней состоят из жидкой фазы и образующегося твердого аустенита. Как определить концентрацию углерода в разных фазах для данного сплава? Рассмотрим для примера сплав с исходной концентрацией углерода 2,5% при температуре 1250°С.
Проведем из этой точки графика «2,5% C – 1250°С» горизонтальную прямую. Пересечение этой прямой с линией AE, граничащей с областью аустенита, покажет концентрацию углерода в аустените при данной температуре (~1.5%).
Пересечение этой же горизонтальной прямой с линией AС, граничащей с областью жидкой фазы, покажет концентрацию углерода в жидкой фазе при данной температуре (~3.5%).
Именно таким образом мы можем определить концентрацию углерода в фазах любого сплава при заданной температуре:
- в жидкой фазе и аустените в области AEC;
- в жидкой фазе в области CDF (концентрация углерода в цементите, конечно, постоянна – 6,67%);
- в аустените в области SEFK;
- в феррите в области QPKL;
- в феррите и аустените в области GPS.
Как видим, при концентрации углерода выше 2,14% насыщение охлаждаемого расплава углеродом всегда стремится к 4,3% (по линиям AC и DC) по мере приближения к температуре 1147°С (уровень ECF). Далее происходит превращение жидкости в ледебурит (эвтектику). Естественно, с этим же средним содержанием углерода.
По мере приближения к температуре 727°С (уровень PSK) концентрация углерода в аустените («свободном» и/или входящем в состав ледебурита) стремится к 0,8% (по линиям GS и ES). Далее происходит превращение аустенита в перлит (эвтектоид). Перлит, конечно, имеет среднее содержанием углерода 0,8%.
Описание
Концентрация углерода в цементите — 6,67% по массе — предельная для железоуглеродистых сплавов. Цементит — метастабильная фаза; образование стабильной фазы — графита во многих случаях затруднено. Цементит имеет орторомбическую кристаллическую решётку, очень твёрд и хрупок, слабо магнитен до 210 °C.
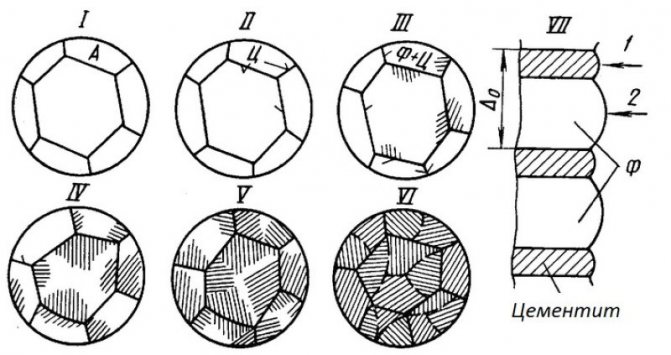
В зависимости от условий кристаллизации и последующей обработки цементит может иметь различную форму — равноосных зёрен, сетки по границам зёрен, пластин, а также видманштеттову структуру.
Цементит в разных количествах, в зависимости от концентрации, присутствует в железоуглеродистых сплавах уже при малых содержаниях углерода. Формируется в процессе кристаллизации из расплава чугуна. В сталях выделяется при охлаждении аустенита или при нагреве мартенсита. Цементит является фазовой и структурной составляющей железоуглеродистых сплавов, составной частью ледебурита, перлита, сорбита и троостита. Цементит — представитель так называемых фаз внедрения, соединений переходных металлов с лёгкими металлоидами. В фазах внедрения велики доля как ковалентной, так и металлической связи.
Твёрдость по Бринеллю больше 800 кг/мм2. Первичный цементит кристаллизуется из жидкого сплава Вторичный цементит — из аустенита Третичный цементит — из феррита
Это интересно: Цементация стали в домашних условиях графитом и другими методами — разбираем досконально
Аустенит в сталях
Наличие аустенита в стальных сплавах придает им определенные свойства. Детали и узлы, произведенные из подобных сталей, предназначаются для работы в средах, содержащие агрессивные компоненты, например, на предприятиях, перерабатывающих разные кислоты.
Стали этого класса отличаются высоким уровнем легирования, во время кристаллизации формируется гранецентрированная решетка. Такая структура не подвержена изменению даже под воздействием глубокого холода.
Стали этого типа можно разделить на два типа отличающиеся друг от друга составом. В первых, содержатся такие вещества как железо, никель, хром. При этом общее количество добавок не может превышать 55%. Ко второй группе относят никелевые и железоникелевые композиции. В никелевых композициях, его содержание превышает 55%. В железоникелевых составах соотношение никеля и железа составляет 1:5, а количество никеля начинается от 65%.
Такое количество никеля обеспечивает повышенную пластичность, а хром, в свою очередь обеспечивает высокую коррозионную стойкость и жаропрочность. Применение других легирующих материалов позволяет выплавлять сплавы с уникальными эксплуатационными свойствами. Металлурги, составляя рецептуру сплавов, руководствуются будущим назначением сталей.
Для получения легированный сталей применяют ферритизаторы, которые придают постоянство аустенитам, к таким веществам относят ниобий, кремний и некоторые другие. Кроме них применяют углерод, марганец – их называют аустенизаторами.
Физика 8 класс. Плавление и кристаллизация
Физика 8 класс Конспект ПлавлениеПлавление и кристаллизация. Удельная теплота плавления.
Задачи на тему Тепловые явления
Переход вещества из твердого состояния в жидкое называется плавлением.
Плавление кристаллических тел происходит только при определенной температуре.
Температуру, при которой вещество плавится, называют температурой плавления вещества.
Чтобы провести процесс плавления, сначала надо нагреть твердое тело до температуры плавления.
Если тело нагреть до температуры плавления и убрать нагреватель (перестать подводить тепло к телу) — то плавления не происходит.
Чтобы осуществить плавление тела, надо выполнить два условия: 1. нагреть тело до температуры плавления 2. продолжить передачу теплоты
Температура плавления — важная тепловая характеристика вещества. У разных веществ температура плавления различна.

Плавление металла
Переход вещества из жидкого состояния в твердое называют отвердеванием или кристаллизацией.
Чтобы началась кристаллизация расплавленного (жидкого) тела, оно должно остыть до определенной температуры.
Температура, при которой вещество отвердевает (кристаллизуется), называют температурой отвердевания или кристаллизации.
График плавления и отвердевания кристаллических тел.
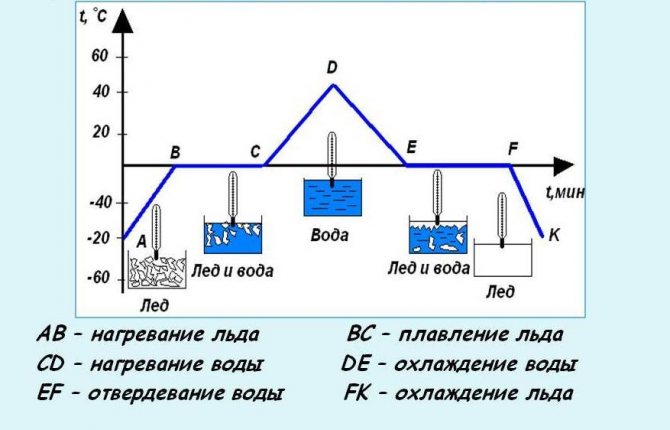
График плавления и отвердевания
Опыт показывает, что вещества отвердевают при той же температуре, при которой плавятся.
Чтобы осуществить процесс отвердевания нужно выполнить два условия: 1. охладить жидкость до температуры отвердевания (плавления) 2. продолжать отводить тепло до тех пор, пока вся жидкость не отвердеет.
Физическая величина, показывающая, какое количество теплоты необходимо сообщить кристаллическому телу массой 1 кг, чтобы при температуре плавления полностью перевести его в жидкое состояние, называется удельной теплотой плавления.
Удельную теплоту плавления обозначают буквой λ, измеряют в Дж/кг.
Чтобы вычислить количество теплоты Q, необходимое для плавления кристаллического тела массой m, взятого при его температуре плавления и нормальном атмосферном давлении,
нужно удельную теплоту плавления λ умножить на массу тела:
где Q– количество теплоты, m– масса тела.
Температура плавления и кристаллизации для данного вещества при неизменном внешнем давлении равны.

Кристаллизация
Количество теплоты, выделяющееся при кристаллизации вещества, при неизменном внешнем давлении равно количеству теплоты, полученному этим веществом при плавлении.
Задачи
Испарение и конденсация
Конспект составлен на основании теоретического материала учебника «Физика 8 класс» А.В. Перышкин, «Физика 8 класс»А.В.Грачев.
Скачать конспект:
teoriya_8_plavleniekristallizacziya
Физика 8 класс. Количество теплоты. Удельная теплоемкость. Топливо.
Физика 8 класс. Кипение. Конденсация.
Физика 8 класс. Испарение. Насыщенный пар. Влажность воздуха.
Физика 8 класс. Тепловые явления. Внутренняя энергия.
Фазы в системе «железо-углерод»
В системе железо – углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
Жидкая фаза
Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
Феррит
Феррит (Ф, α)- твердый раствор внедрения углерода в α-железе (от латинского слова ferrum – железо). Различают низкотемпературный феррит с предельной растворимостью углерода 0,02 % при температуре 727° С (точка P) и высокотемпературный δ-феррит (в интервале температур 1392…1539° С) с предельной растворимостью углерода 0,1 % при температуре 1499° С (точка J).
Свойства феррита близки к свойствам железа. Он мягок (твердость – 80 — 130 НВ, временное сопротивление – σв=300 МПа) и пластичен (относительное удлинение — δ=50 %), магнитен до 768° С.
Под микроскопом феррит выглядит как светлые полиэдрические зерна. В сталях может существовать в виде сетки (разной толщины, в зависимости от содержания углерода), зерен (малоуглеродистые стали), пластин или игл (видманштетт).
Аустенит в сталях
Аустенит (А, γ) – твердый раствор внедрения углерода в γ–железо (по имени английского ученого Р. Аустена). Углерод занимает место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в γ -железе 2,14 % при температуре 1147° С (точка Е). Аустенит имеет твердость 180 НВ, пластичен (относительное удлинение – δ=40…50 %), парамагнитен. При растворении в аустените других элементов могут изменяться свойства и температурные границы существования. Под микроскопом выглядит как светлые полиэдрические зерна с двойниками.
Цементит – формы существования
В железоуглеродистых сплавах присутствуют фазы: цементит первичный, цементит вторичный, цементит третичный. Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
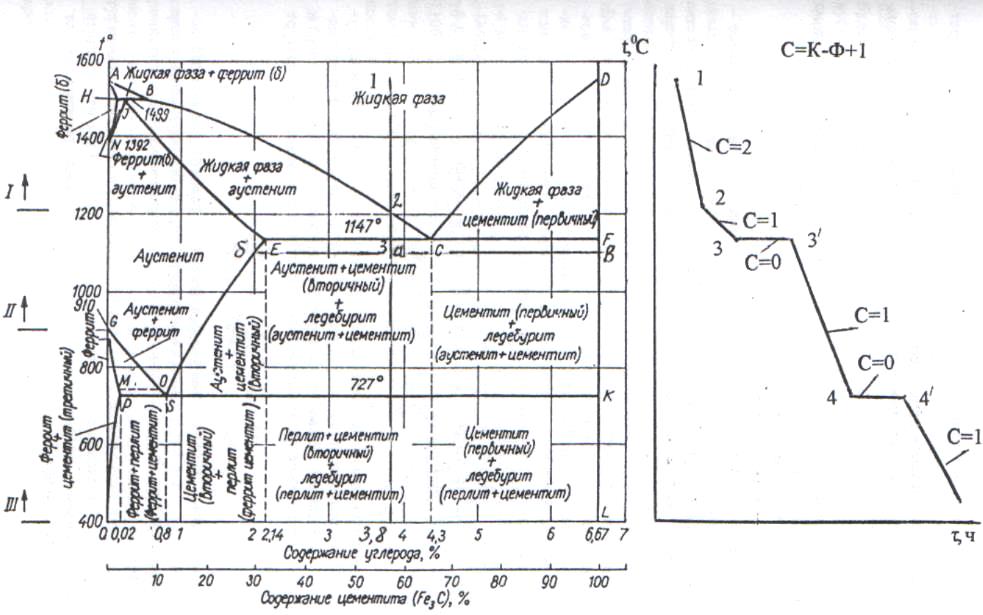
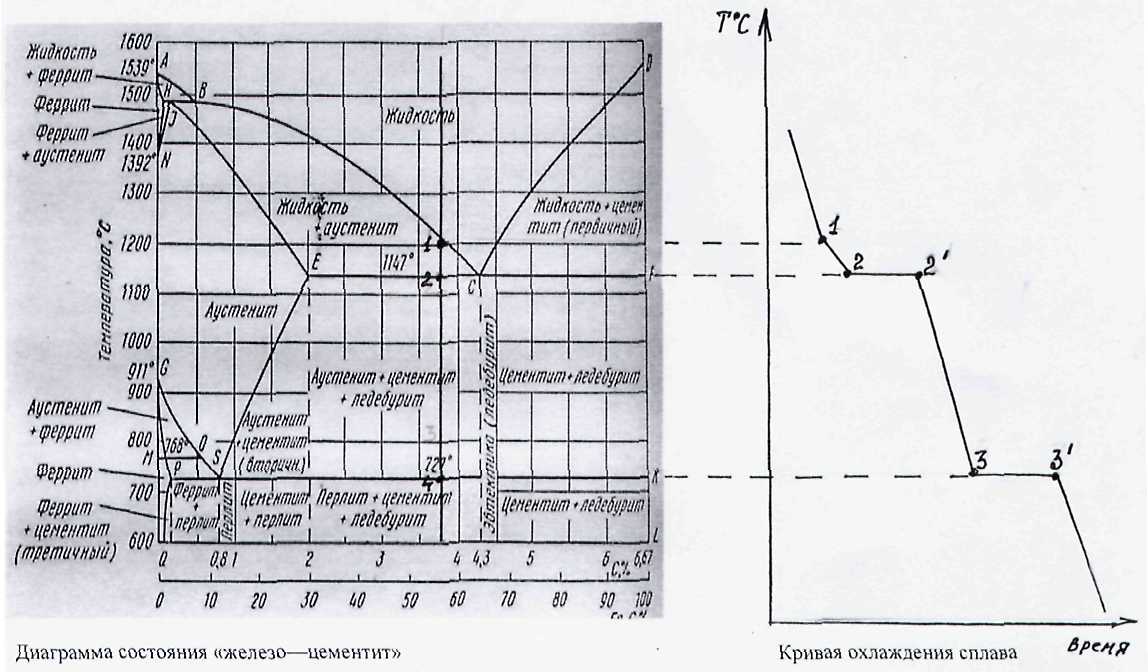
Поскольку углерод в сплавах с железом встречается в виде цементита и графита, существуют две диаграммы состояния, описывающие условия равновесия фаз в системах железо — цементит и железо — графит. Первая диаграмма (Fе — Fе3С) называется цементитной (метастабильная), вторая (Fе — С) — графитной (стабильная). Оба варианта диаграммы приводятся вместе в одной системе координат: температура — содержание углерода. Диаграмма состояния системы железо — углерод построена по результатам многочисленных исследований, проведенных учеными ряда стран. Особое место среди них занимают работы Д.К. Чернова
Он открыл существование критических точек в стали, определил их зависимость от содержания углерода, заложил основы для построения диаграммы состояния железоуглеродистых сплавов в ее нижней, наиболее важной части
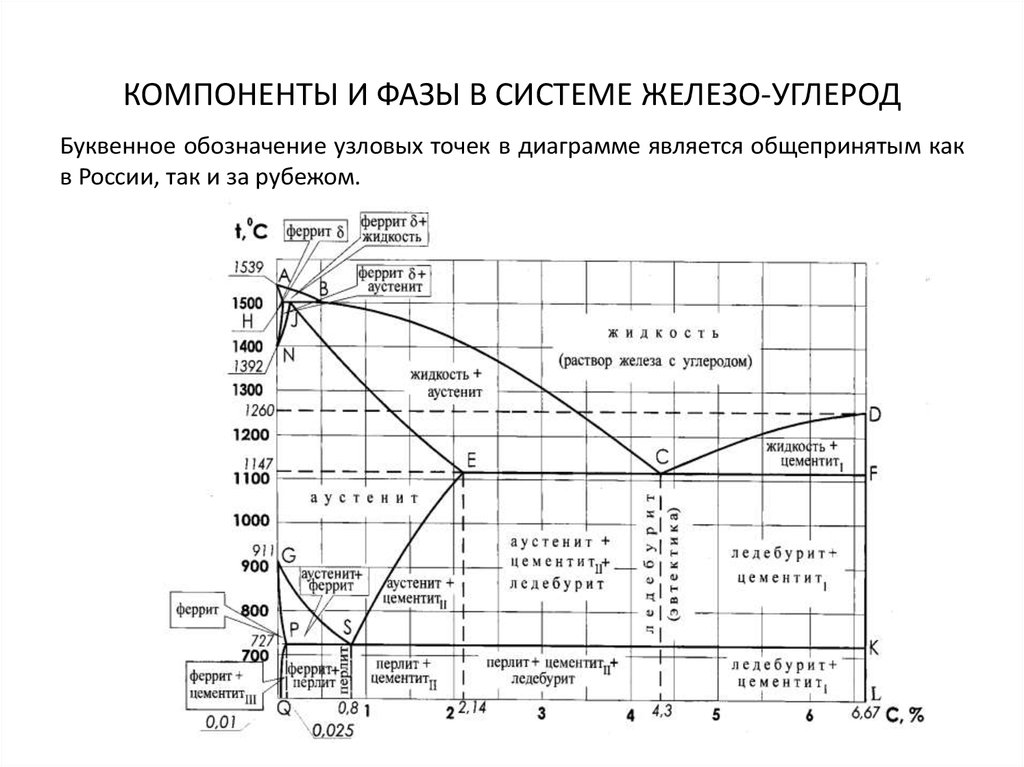
Буквенное обозначение узловых точек в диаграмме является общепринятым как в России, так и за рубежом.
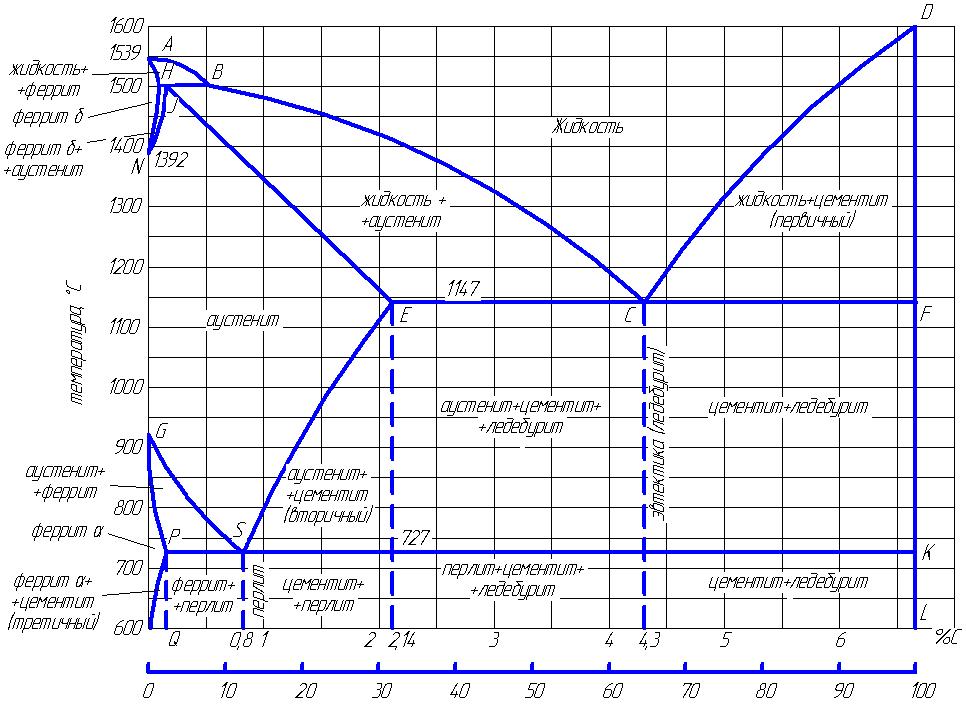
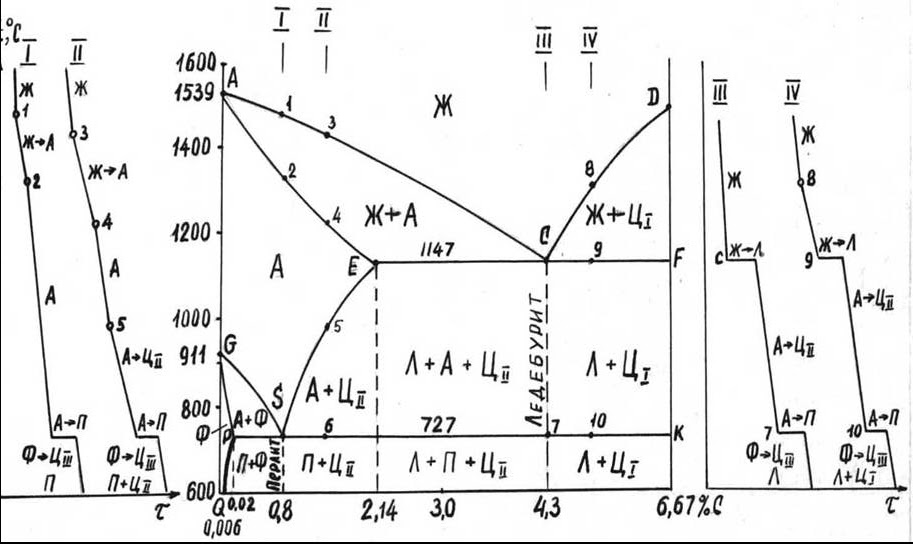
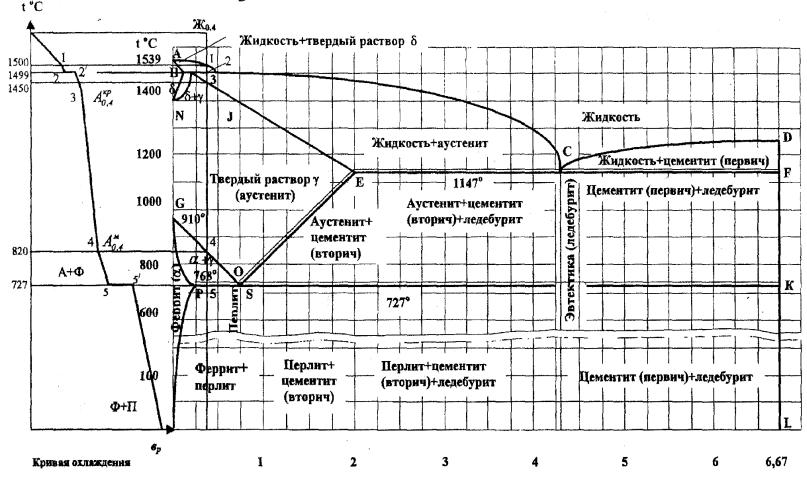
Диаграмма состояния железо-углерод
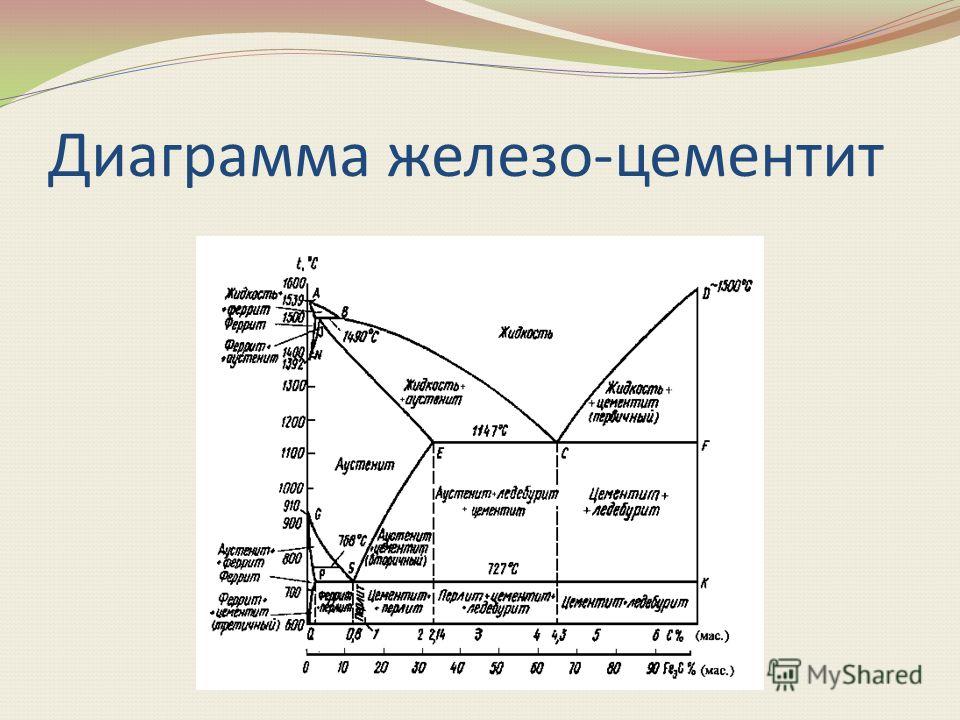
Имеющиеся во всех областях диаграммы фазы видны на рисунке. Значение всех линий указано в таблице.
Ликвидус по всей диаграмме проходит по линиям АВ, ВС, СD; солидус — по линиям АН, НJ, JЕ, ЕСF. Сплавы железа с углеродом обычно делят на стали и чугуны. Условной границей для такого деления является 2,14 % С (точка E). Сплавы, содержащие углерода менее 2,14 %, относятся к сталям, более 2,14 % — к чугунам.
Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо – цементит, т.е. критические точки, имеют условные обозначения. Обозначаются буквой А. В зависимости от того, при нагреве или при охлаждении определяется критическая точка, к букве А добавляется индекс с (от слова chauffage – нагрев) при нагреве и индекс r (от слова refroidissement – охлаждение) при охлаждении с оставлением цифры, характеризующей данное превращение.
Таким образом, например, нагрев доэвтектоидной стали выше соответствующей точки на линии GS обозначается как нагрев выше точки АС3. При охлаждении же этой стали первое превращение должно быть обозначено как Аr3, второе (на линии РSК) — как Аr1.
Классификация железоуглеродистых сплавов
Классификация железоуглеродистых сплавов в зависимости от концентрации углерода в сплаве:
- C<0,025%. Техническое железо. При комнатной температуре будет состоять только из феррита;
- 0,025<C<2,14. Стали:
- 0,025<C<0,8. Доэвтектоидные стали. Состав: феррит + перлит (или третичный цементит);
- C=0,8. Эвтектоидная сталь. «Чистый» перлит;
- 0,8<C<2,14. Заэвтектоидная сталь. Состав: вторичный цементит + перлит;
- 2,14<C<6,67. Чугуны:
- 2,14<C<4,3. Доэвтектический чугун. Состав: ледебурит + перлит + вторичный цементит;
- C=4,3. Эвтектический чугун. «Чистый» ледебурит;
- 4,3<C<6,67. Заэвтектический чугун. Состав: ледебурит + цементит.
Техническое железо выделяет то, что оно состоит исключительно из феррита. Который и определяет его свойства: мягкость, чрезвычайную пластичность и т.д.
Чугуны же выделяет наличие ледебурита, придающего им хрупкость. Поэтому чугуны не могут подвергаться ковке. Зато обладают лучшими литейными свойствами (чем стали), обусловленными наличием легкоплавкого ледебурита.
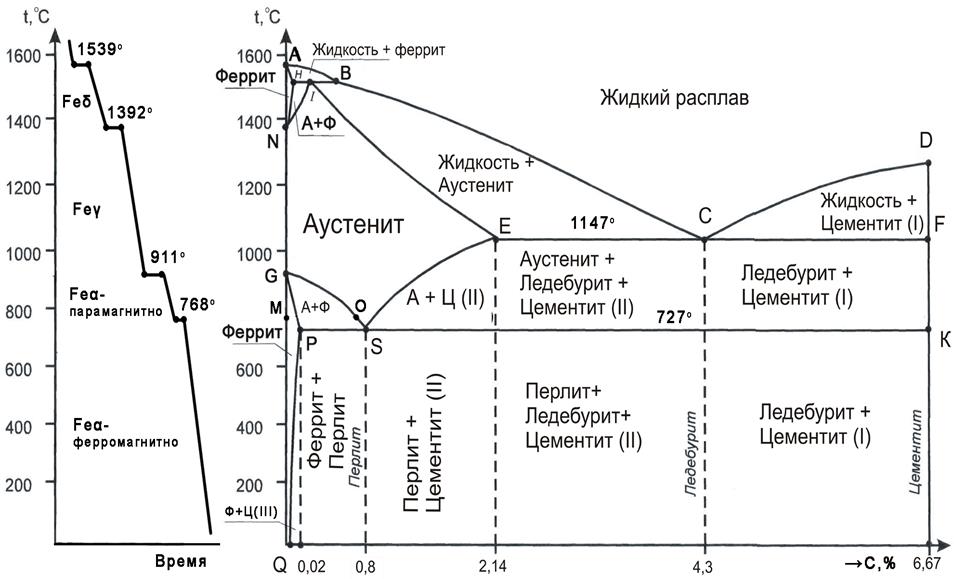
Диаграмма состояния [ править | править код ]
Железо образует с углеродом химическое соединение Fe3C цементит. Так как на практике применяют металлические сплавы на основе железа с содержанием углерода до 5 %, практически интересна часть диаграммы состояния от чистого железа до цементита . Поскольку цементит — метастабильная фаза, то и соответствующая диаграмма называется метастабильной (сплошные линии на рисунке).
Для серых чугунов и графитизированных сталей рассматривают стабильную часть диаграммы железо—графит (Fe—Гр), поскольку именно графит является в этом случае стабильной фазой. Цементит выделяется из расплава намного быстрее графита и во многих сталях и белых чугунах может существовать достаточно долго, несмотря на метастабильность. В серых чугунах графит существует обязательно.
На рисунке тонкими пунктирными линиями показаны линии стабильного равновесия (то есть с участием графита), там где они отличаются от линий метастабильного равновесия (с участием цементита), а соответствующие точки обозначены штрихом. Обозначения фаз и точек на этой диаграмме приведены согласно неофициальному международному соглашению.
Другие структурные составляющие в системе «железо-углерод»
Кроме компонентов и фаз в системе сплавов «железо-углерод» присутствуют другие структурные составляющие — перлит и ледебурит
Перлит
Перлит — эвтектоид, механическая смесь феррита и цементита, полученная в результате распада аустенита при охлаждении сплавов ниже 727° С. При медленном охлаждении перлит присутствует во всех сплавах с концентрацией углерода от 0,02 до 6,67%. Под микроскопом перлит может выглядеть либо как пластины, либо как зерна — зернистый перлит. Его вид, также как и механические свойства, зависит от скорости охлаждения сплава и вида его термической обработки
Ледебурит в сталях
Ледебурит — эвтектика, механическая смесь аустенита и цементита, выделяющаяся из жидкости при охлаждении сплавов ниже 1147° С. Принципиальное отличие эвтектикой составляющей от эвтектоидной заключается в том, что первая выделяется из жидкости, а вторая из твердого раствора, в случае железоуглеродистых сплавов — из аустенита. Название данная структурная составляющая получила в честь имени немецкого ученого-металлурга Ледебура.
Это интересно: Чем и как очистить медь в домашних условиях
Полиморфные превращения
Более подробно о каждой фазе чуть ниже в статье. А если кратко, то осуществление главных превращений происходит при особых температурах.
Состояние железа обозначают как α-феррум (при температуре менее 911° С) . Кристаллическая решетка – объемный гранецентрированный куб. Или ОЦК. Дистанция между атомами такой решетки достаточно высокая.
Железо приобретает модификацию гамма, то есть обозначается как γ-феррум (911-1392° С) . Кристаллическая решетка – гранецентрированный куб (ГЦК). В этой решетке дистанция между атомами ниже, чем в ОЦК.
При переходе α-феррума в γ-феррум объем вещества становится меньшим. Причиной тому является кристаллическая решетка – ее вид. Потому что решетка ГЦК имеет более упорядоченное состояние атомов, чем ОЦК.
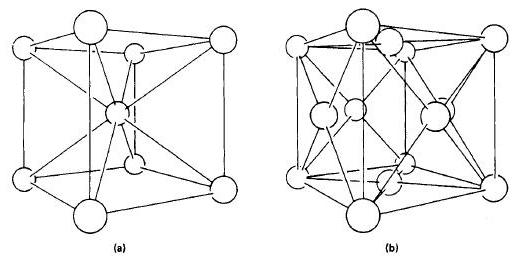
Если переход осуществляется в обратном направлении – из γ-феррума в α-феррум, то объем сплава увеличивается.
Когда температура достигает значения 1392° С (но менее температуры плавления железа 1539° С), то α-феррум превращается в δ-феррум, но это не является ее новой формой, а лишь разновидностью. К тому же δ-феррум является неустойчивой структурой.
Химические свойства
Как химическое соединение цементит обладает своими физическими, химическими и механическими характеристиками. Он имеет серый кристаллический вид на изломе, относительно твёрдый с высокой термической устойчивостью. Основные химические свойства цементита выражаются в следующих показателях:
- химическая формула Fe3C;
- разложение структуры происходит при температуре более 1650°С;
- подвержен воздействию различных кислот (особенно высоко концентрированных);
- быстро вступает в реакцию с кислородом.
На основании существующих химических свойств сформированы физические и механические свойства. К основным физическим свойствам относятся:
- температура плавления равняется 1700 °С;
- молекулярная масса составляет 179,55 а.е.м.;
- плотность цементита равна 7,7 г/см3 при температуре равной 20 °С.
К основным механическим свойствам относятся:
- твердость;
- стойкость к ударным воздействиям (хрупкость);
- сопротивление на излом;
- пластичность.
Твёрдость этого соединения достигает больших значений и равна НВ 8000 МПа или HRC 70. Однако он обладает достаточной хрупкостью и низкой пластичностью.
Обладая перечисленными свойствами, цементит активно используется при производстве литых деталей различного назначения. Образование различного вида цементита и его соединений с другими формами приводит к изменению характеристик получаемой стали или чугуна, следовательно, к улучшению или снижению отдельных потребительских свойств.
Например, для получения белого чугуна и придания ему высокой прочности и пластичности стараются перевести цементит в графит. Это достигается при проведении операции отжига. При возрастании температуры он распадается на две составляющие: феррит и графит.
В зависимости от требуемых свойств в чугуне стараются сохранить требуемое количество цементита. Особенно это касается так называемого свободной фракции этого соединения. Для снижения его концентрации применяют различные способы химической и термической обработки. Для решения этой задачи применяют раствор азотной кислоты в чистом спирте. Структурно свободный цементит выпадает в осадок в результате кипячения чугунной болванки в этом растворе. Кроме этого применяют три вида обработки: отжиг, нормализацию и закалку.
Техническое железо содержит третичный цементит в сочетании с ферритом. Он проявляется по границе феррита при содержании углерода от 0,01% до 0,025%. Для повышения качества стали стараются снизить содержание свободного цементита. Особенно его концентрация наблюдается в мягких марках стали. Большое влияние на качество штамповки оказывает содержание этой смеси и перлита в единице объёма. Излишнее присутствие третичного цементита, особенно в форме продолжительной цепочки или сетки приводит к образованию разрывов во время штамповки. Поэтому для получения хорошей ковочной стали стараются снизить количество третичного цементита. Структура таких образований не должна превышать второго балла по установленной шкале. Получаемая твёрдость не должна превышать HB 50 единиц.
Цементит: формы существования
Так называют соединение углерода и железа. Это компонент чугуна и некоторых сталей. В него входит 6,67% углерода.
В его кристалл входит несколько октаэдров, они расположены друг по отношению к другу с некоторым углом. Внутри каждого из них расположен атом углерода. В результате такого построения получается следующая картина – один атом вступает в связь с несколькими атомами железа, а железо в свою очередь связано с тремя атомами этого элемента.

Кристаллическая решетка цементита
У этого вещества имеются все свойства, которые присущи металлам – электропроводность, своеобразным блеском, высокая теплопроводность. То есть, смесь железа и углерода, ведет себя как металл. Этот материал обладает определенной хрупкостью. Большая часть его свойств определена сложным строением кристаллической решетки.
Этот материал плавится при 1600 градусах Цельсия. Но на этот счет существует несколько мнений, одни исследователи считают, что его температура плавления лежит в диапазоне от 1200 до 1450, другие определяют, что верхний уровень равен 1300 °С.
Первичный цементит
Металлурги разделяют три типа этого вещества – первичный, вторичный, третичный.
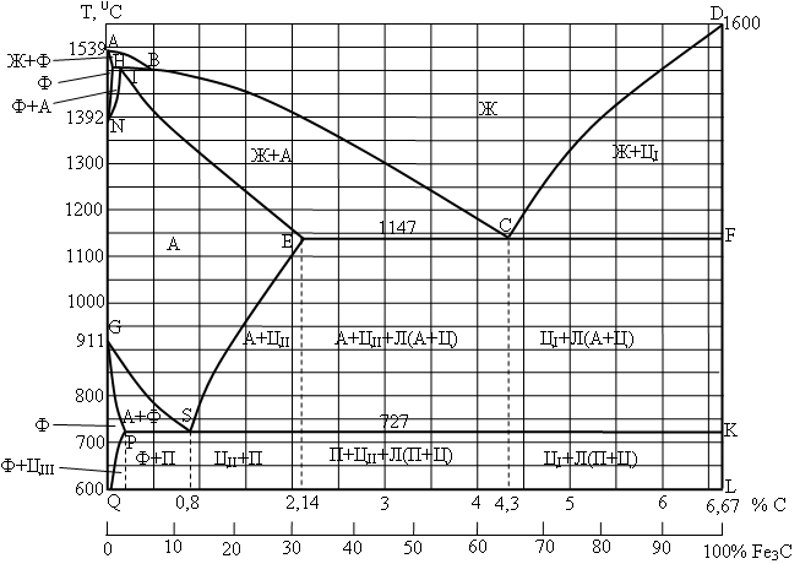
Диаграмма железо-цементит
Первичный, получается из жидкости при закалке сплавов, которые содержат в себе 5,5% углерода. Первичный имеет форму в виде крупных пластин.
Вторичный
Этот элемент получается из аустенита при охлаждении последнего. На диаграмме этот процесс этот процесс можно видеть по диаграмме Fe – C. Цементит представлен в виде сетки, размещенной по границам зерен.
Третичный
Этот тип, является производным от феррита. Он имеет форму иголок.
В металлургии существуют и другие формы цементита, например, цементит Стеда и пр.
Другие структурные составляющие в системе железо углерод
Перлит
Перлит – это механическая смесь, которая состоит из феррита и цементита. Ледебурит представляет собой переменный раствор.

Перлит
При температуре от 1130 и до 723 °С в его состав входят аустенит и цементит. При более низких температурах он состоит из аустенит заменяет феррит.
Компоненты в системе железо углерод
Аустенит
Атомы размещается в гранецентрированной ячейке. Твердость аустенита имеет твердость 200 … 250 единиц по Бринеллю. Кроме того у него хорошая пластичность и он отличается парамагнитностью.
Железо
Железо – это материал, относящийся к металлам. Его натуральный цвет – серебристо-серый. В чистом виде он очень пластичен. Его удельный вес составляет 7,86 г/куб. см. Температура плавления составляет 1539 °C. На практике чаще всего применяют техническое железо, в составе которого присутствуют следующие примеси – марганец, кремний и многие другие. Массовая доля примесей не превышает 0,1%.

Железо
У железа есть такое свойство как полиформизм. То есть, при одном и том же химическом составе, это вещество может иметь разную структуру кристаллической решетки и соответственно разные свойства. Модификации железа называют соответственно – Б, Г, Д. Все эти модификации существуют при разных условиях. Например, тип Б, может существовать только при температуре 911 °С. Тип Г может существовать в диапазоне от 911 до 1392 °С. Тип Д существует в диапазоне от 1392 до 1539 °С.
Каждый из типов обладает своей формой кристаллической решеткой, например, у типа Б решетка представляет собой куб, решетка типа Г имеет гранецентрированную кубическую форму. Решетка типа Д, имеет форму объемно центрированного куба.
Еще одно свойство состоит в том, что при температуре ниже 768 железо ферримагнитно, а при ее повышении это свойство теряется.
Точки полиморфной и магнитной трансформации называют критическими. На таблице они обозначены следующим образом – А2, А3, А4. Цифровые индексы показывают тип трансформации. Для более полного различия превращения железа из одного вида в другой к обозначению добавляют индексы с и r. Первый говорит о нагреве, второй об охлаждении.

Полиморфные модификации железа
При высоких параметрах пластичности, железо не обладает высокой твердостью, по шкале Бринелля она равна 80 единиц.
Железо имеет возможность образовывать твердые растворы. Их можно разделить на две группы – раствор замещения и внедрения. Первые состоят их железа и других металлов, вторые из железа и углерода, водорода и азота.
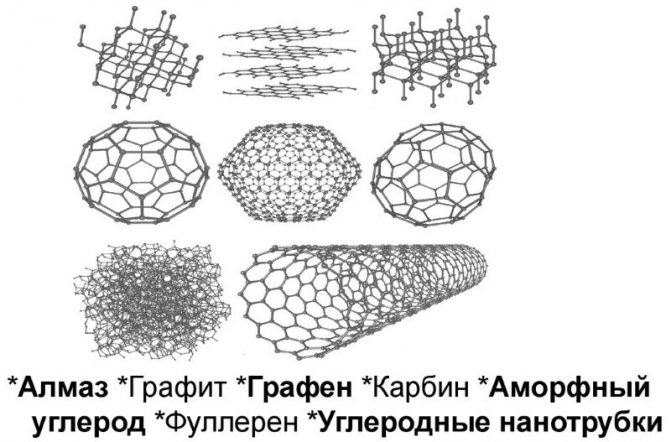
Углерод
Другой компонент системы – углерод. Это – неметалл и он обладает тремя модификациями в виде алмаза, графита и угля. Он плавится при 3500 °С.
Аллотропные модификации углерода
В сплаве железа, этот элемент находится в виде твердого раствора, его называют цементит или в виде графита. В таком виде он присутствует в сером чугуне. Графит, не отличается ни пластичностью, ни прочностью.
Цементит
Доля углерода составляет 6,67%. Он обладает высокой твердостью – 800 НВ, но при этом у него отсутствует пластичность. Полиморфными свойствами не обладает.
Он обладает следующим свойством – при формировании раствора замещения, углерод может быть заменен на атомы других веществ, например, на хром или никель. Такой раствор получил название легированного раствора.

Цементит
Он не обладает устойчивостью, при наличии некоторых условий он может разлагаться, при этом происходит трансформация углерода в графит. Это свойство нашло применение при образовании чугунов.
Кстати, в жидком состоянии, железо может растворять в себе примеси, при этом образуя, однородная масса.
Феррит
Так называют твердый раствор, при котором происходит внедрение углерода в железо.
Он растворяется с определенной переменностью, при нормальной (комнатной) температуре объем углерода лежит в пределах 0,006%, при 727 °С, то концентрация углерода составит 0,02%. По достижении 1392 °С образуется феррит.
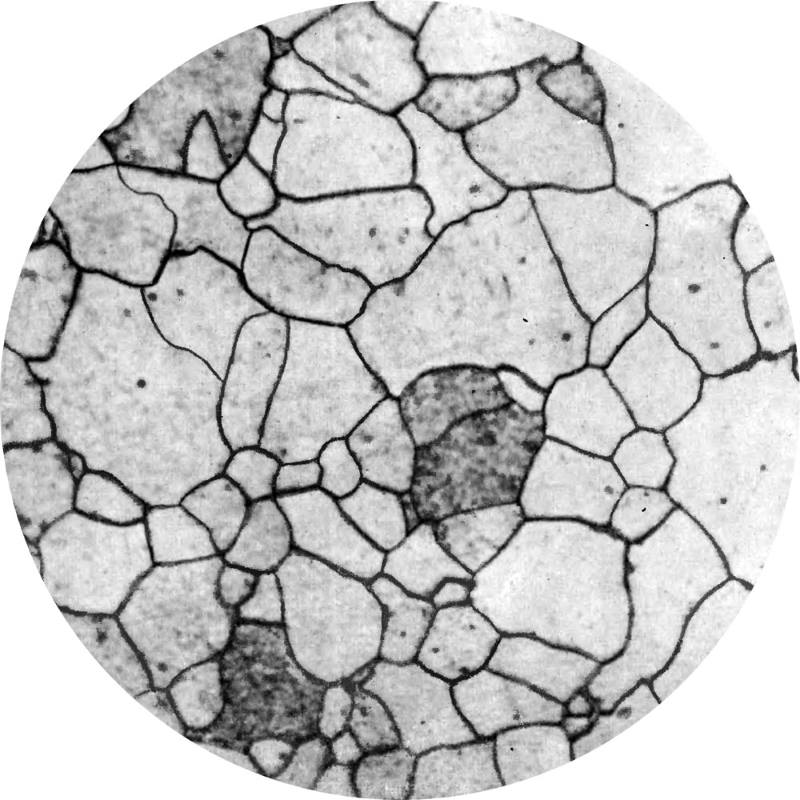
Феррит
Содержание углерода составит 0,1%. Его атомы размещаются в дефектных узлах решетки.
Феррит по своим параметрам близок к железу.
Фазы в системе “железо-углерод”
Фазы – это физически однородные состояния сплава. Фаза имеет точный химический состав – определенное расположение и связь между атомами. Такая структура атомов придает разные свойства различным фазам.
Некоторые специальные сплавы могут существовать в нескольких фазах, что достигается нагревом металла до определенных температур и использованием разных процедур термообработки.
Жидкая
Существует при температуре, которая превышает 1457 oC. Фазовое превращение при этой температуре означает полное плавление, поэтому на диаграмме жидкая фаза всегда обозначается линией L.
Феррит
На диаграмме присутствует в трёх разных фазах:
- Фаза дельта-феррита (δ-Fe) представляет собой твердый раствор C в δ-Fe (ОЦК) в высокотемпературной области диаграммы. Раствор стабилен при температуре выше 1400 °C и плавится при температуре выше 1539 °C. Структурно подобен α-ферриту;
- Фаза гамма-феррита (γ-Fe) является твёрдым раствором C в γ-Fe, который называют аустенитом. Нестабилен ниже температуры 910 °C, превращаясь в δ-феррит при 1395 ° C.. Максимальная растворимость углерода составляет около 2,1% при 1147 °C. Аустенит мягок и пластичен, не обладает магнитными свойствами;
- Фаза альфа-феррита (α-Fe) представляет собой твердый раствор C в α-Fe с ОЦК-решёткой. Считается самой стабильной формой железа при комнатной температуре. Максимальная растворимость углерода составляет около 0,02% при 727 °C. Мягче аустенита, магнитен.
Аустенит в сталях
Аустенит всегда присутствует в нержавеющих сталях, которые содержат от 16 до 26 процентов хрома и до 35 процентов никеля. Аустенитные стали, помимо высокой коррозионной стойкостью, не закаливаются при термической обработке и немагнитны.
Формы существования цементита важны для определения коррозионной стойкости сталей. Доказано, что цементит (Fe3C) увеличивает скорость коррозии, причём этот эффект более выражен, когда он образует когерентную сеть на поверхности. В нормализованных сталях цементит образует когерентную сетку, а в отпущенном мартенсите – нет. Поэтому цементит влияет на скорость коррозии нормализованной, но не закалённой стали.
В целом скорость коррозии углеродистой стали снижается с увеличением содержания хрома из-за образования защитного оксида хрома. Однако, когда хром соединяется с углеродом с образованием карбида хрома, положительный эффект хрома теряется.
Чугуны
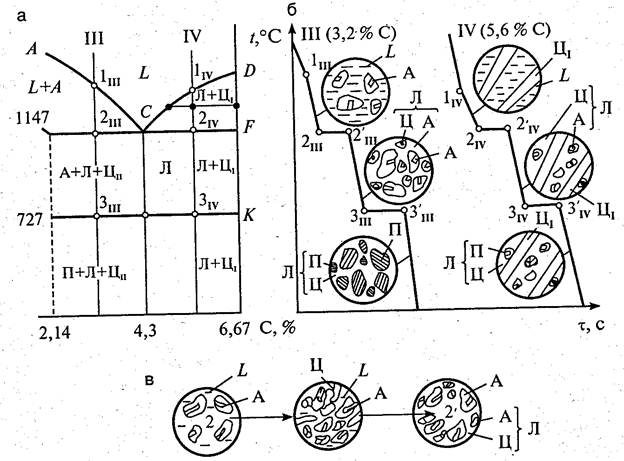
Сплавы на диаграмме железо-углерод, которые содержат углерода более, чем 2,14 %, называются чугунами. Они обладают высокой хрупкостью. Поперечное сечение такого чугуна имеет светлый тон, а потому его называют белым чугуном.
На диаграмме это точка С, называемая эвтектикой, с соответствующим содержанием углерода 4,3 %. При кристаллизации образуется смесь, состоящая из аустенита и цементита, в совокупности называемая ледебуритом. Фазовый состав постоянен.
При концентрации углерода менее 4,3 % (доэвтектический чугун) при кристаллизации выделяется аустенит из раствора. Далее из него выделяется Ц2. А при 727° С аустенит превращается в перлит. Структурное состояние такого чугуна следующее: крупные участки перлита темного тона.
В заэвтектическом белом чугуне (углерода более 4,3%) при охлаждении структурирование происходит с образованием кристаллов Ц1. Далее превращения осуществляются уже в твердом состоянии. Структура представляет собой ледебурит, который является фоном для полей перлита темного тона. А крупные пласты – это Ц1.