История открытия
В конце 18 столетия Ю. Гадолином было получено первое соединение из группы редкоземельных металлов – оксид иттрия. До начала 20 столетия благодаря исследованиям Г. Мозли в химии стало известно о существовании группы металлов. Они располагались в периодической системе между лантаном и гафнием. Еще один химический элемент – актиний, подобно лантану, образует семейство из 14 радиоактивных химических элементов, названных актиноидами. Их открытие в науке произошло, начиная с 1879 года до середины 20 века. Лантаноиды и актиноиды имеют достаточно много черт сходства как в физических, так и в химических свойствах. Это можно объяснить расположением электронов в атомах этих металлов, которые находятся на энергетических уровнях, а именно для лантаноидов это четвертый уровень f-подуровень, а для актиноидов – пятый уровень f-подуровень. Далее мы рассмотрим электронные оболочки атомов вышеназванных металлов более подробно.
Индивидуальные доказательства
- Вольфганг Либшер, Эккехард Флюк: Систематическая номенклатура неорганической химии . Springer-Verlag, Берлин 1999, ISBN 3-540-63097-X .
- Номенклатура неорганической химии, Рекомендации ИЮПАК 2005 .
- AM Mariano: Экономическая геология редкоземельных минералов . В: Б. Р. Липин, Г. А. Маккей (ред.): Обзоры по минералогии , том 21 – Геохимия и минералогия редкоземельных элементов (1989). Опубликовано Минералогическим обществом Америки, ISBN 0-939950-25-1 , стр. 309-337.
- Георг Штайнхаузер : Структурная химия – Прикосновение к пустоте. В кн . : Новости химии. 66, 2018, стр 118,. DOI : .
- А. Ф. Holleman , Е. Wiberg , Н. Wiberg : Учебник неорганической химии . 102-е издание. Вальтер де Грюйтер, Берлин 2007, ISBN 978-3-11-017770-1 , стр. 1937.
- ДТВ атлас по химии . 1981 , часть 1. С. 220.
- ↑
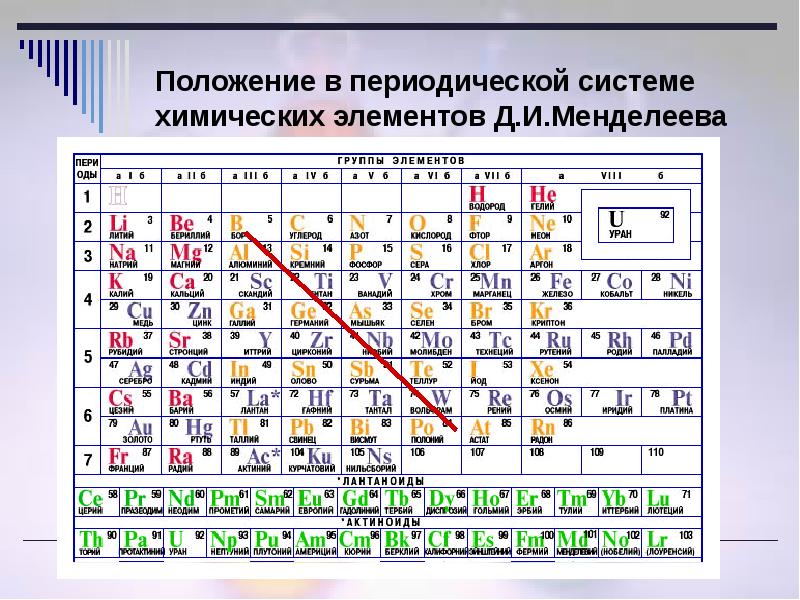
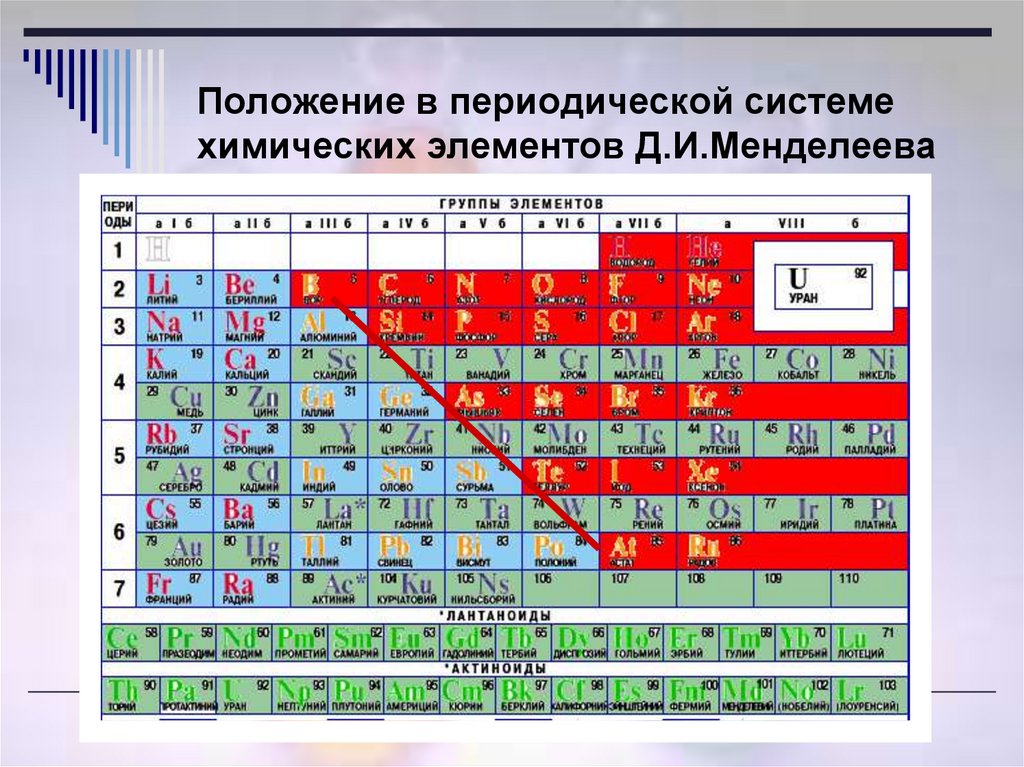
Положение в периодической системе водорода, лантаноидов, актиноидов
Нужно учитывать тот факт, что водород является достаточно реакционноспособным веществом. Он проявляет себя в зависимости от условий химической реакции: как восстановителем, так и окислителем. Именно поэтому в периодической системе водород располагается одновременно в главных подгруппах сразу двух групп.
В первой водород играет роль восстановителя, как и щелочные металлы, расположенные здесь. Место водорода в 7-й группе наряду с элементами галогенами указывает на его восстановительную способность. В шестом периоде находится, как уже ранее было сказано, семейство лантаноидов, вынесенное в отдельный ряд для удобства и компактности таблицы. Седьмой период содержит группу радиоактивных элементов, по своим характеристикам подобным актинию. Актиноиды располагаются вне таблицы химических элементов Д.И Менделеева под рядом семейства лантана. Эти элементы наименее изучены, так как ядра их атомов очень неустойчивы по причине радиоактивности. Напомним, что лантаноиды и актиноиды относятся к элементам внутренним переходным, а их физико-химические характеристики очень близки между собой.
Нахождение в природе
С точки зрения нахождения в природе лантаноиды делятся на 2 группы: цериевую ( Ce, Pr, Nd, Pm, Sm, Eu) и иттриевую ( Gd, Tb, Dy, Ho, Er, Tm, Yb, Lu). Данный раздел основывается на том, что в одних минералах встречаются преимущественно церий и его “группа”, а в других – иттрий вместе с остальными элементами. К минералам цериевой группы относится монацит (Это, La, Nb ….) PO 4. Он образует россыпи монацитового песка, куда, кроме него, входит кварц, рутил, оксид тория. В монацитового песка содержатся все минералы цериевой группы. Элементы этой же группы содержатся в изоморфных фторокарбонатах (Это, La ….) FCO 3 (бастнезит), а также в собственном силикате Ce 2 Si 2 O 7 (церит). К минералам иттриевой группе относится ксенотим (Y, Eu, Gd, …) РО 4, в котором лантаноиды изоморфно замещают друг друга.
Второй по важности редкоземельный минерал – бастнезит – во многом похож на него. Бастнезит тоже тяжелый, тоже блестящий, тоже не постоянен по окраске (чаще всего ярко-желтый). Но химически с монацита его объединяет только большое содержание лантана и лантаноидов
Если монацит – фосфат, то бастнезит – фторокарбонат редких земель, его состав обычно записывают так: (La, Се) FCO 3. Но, как часто бывает, формула минерала не полностью отражает его состав. В данном случае она указывает лишь на главные компоненты: в бастнезити 36,9-40,5% оксида церия и почти столько же (в сумме) оксидов лантана, празеодима и неодима. Но обычно в нем есть и другие лантаноидов
Но химически с монацита его объединяет только большое содержание лантана и лантаноидов. Если монацит – фосфат, то бастнезит – фторокарбонат редких земель, его состав обычно записывают так: (La, Се) FCO 3. Но, как часто бывает, формула минерала не полностью отражает его состав. В данном случае она указывает лишь на главные компоненты: в бастнезити 36,9-40,5% оксида церия и почти столько же (в сумме) оксидов лантана, празеодима и неодима. Но обычно в нем есть и другие лантаноидов.
Есть даже селективный неодимовый минерал – ешинит. В этот минерал входят окислы кальция, тория, тантала, ниобия, иттрия, лантана и лантаноидов, из которых в нем больше церия и неодима.
Лантаноиды распространены в природе не одинаково. Наиболее труднодоступные лантаноиды – тербий, тулий, лютеций (все это лантаноиды с нечетными атомными номерами) – стоят дороже золота и платины.
Ресурсы лантанидов довольно значительны – суммарный массовое содержание лантанидов (вместе с лантаном) в земной коре 0,01%, что близко к содержанию меди. Наиболее распространенными являются La, Ce i Nd. Известно более 250 минералов, содержащих лантаниды. Из них собственных минералов лантанидов – 60-65 (содержание редких земель более 5-8%). Это главным образом фосфаты, лития или флуорокарбонаты, титанониобаты. Важнейшие минералы, содержащие лантаниды: монацит, ксенотим, бастнезит, гадолинит, ортит, лопарит, евксенит, фергусонит, самарскит. Лантаниды концентрируются в различных типах магматогенных, осадочных и метаморфогенных месторождений.
В Украину руды лантанидов не добываются. Потребности страны (ок. 100 т / год) покрывает импорт. Промышленные концентрации лантанидов обнаружены в юго-восточной и юго-западной частях Украинского щита.
Сокращение лантаноидов
→ Основная статья : Сокращение лантаноидов
Из-за сжатия лантаноидов атомный радиус почти непрерывно уменьшается в диапазоне от церия (183 мкм) до лютеция (172 мкм) (исключение составляют европий и иттербий). Это связано с тем, что элементы, которые – в зависимости от атомного номера – находятся перед лантаноидами, уже заполнили электронами оболочки 6s и 5p, но не оболочку 4f. Теперь лантаноиды заполняют 4f-оболочку электронами. В упрощенном представлении атома как состоящего из пространственно разделенных электронных оболочек, электронная оболочка, пространственно более близкая к ядру, теперь заполнена носителями заряда. Вдобавок ядро, конечно, заполнено тем же числом протонов, что и электроны, добавленные к 4f-оболочке. В результате более сильное притяжение между электронами и протонами сокращает атомный радиус, в то время как атомный номер увеличивается.
Этот эффект на самом деле не является исключительным, поскольку радиус всегда уменьшается, когда чаша наполняется в течение определенного периода времени. Однако это свойство имеет некоторые последствия:
- Благодаря уменьшающимся размерам легко возможно разделение с помощью ионообменников .
- В гольмии радиус Ln 3+ настолько мал, что почти соответствует радиусу Y 3+ ; поэтому иттрий обычно встречается вместе с «тяжелыми землями».
- Внутри группы переходные элементы во 2-й и 3-й позициях имеют очень похожие свойства.
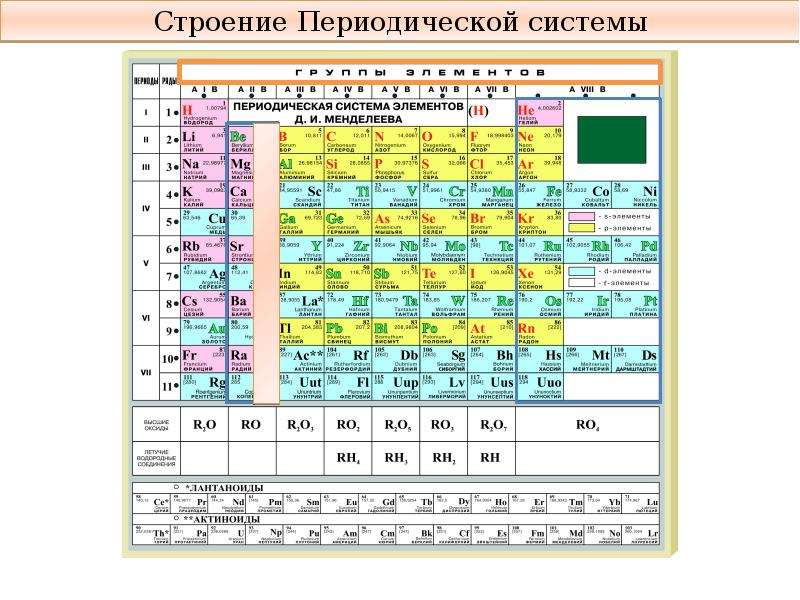
Периодический закон
К середине XIX века учёные располагали множеством сведений о физических и химических свойствах разных элементов и их соединений. Появилась необходимость упорядочить эти знания и представить их в наглядном виде. Исследователи из разных стран пытались создать классификацию, объединяя элементы по сходству состава и свойств веществ, которые они образуют. Однако ни одна из предложенных систем не охватывала все известные элементы.
Пытался решить эту задачу и молодой русский профессор Д.И. Менделеев. Он собирал и классифицировал информацию о свойствах элементов и их соединений, а затем уточнял её в ходе многочисленных экспериментов. Собрав данные, Дмитрий Иванович записал сведения о каждом элементе на карточки, раскладывал их на столе и многократно перемещал, пытаясь выстроить логическую систему. Долгие научные изыскания привели его к выводу, что свойства элементов и их соединений изменяются с возрастанием атомной массы, однако не монотонно, а периодически.
Так был открыт периодический закон, который учёный сформулировал следующим образом: «Свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».

Своё открытие Менделеев совершил почти за 30 лет до того, как учёным удалось понять структуру атома. Открытия в области атомной физики позволили установить, что свойства элементов определяются не атомной массой, а зависят от количества электронов, содержащихся в нём. Поэтому современная формулировка закона звучит так:
Свойства химических элементов, а также формы и свойства образуемых ими веществ и соединений находятся в периодической зависимости от величины зарядов ядер их атомов.
Этот принцип Менделеев проиллюстрировал в таблице, в которой были представлены все 63 известных на тот момент химических элемента. При её создании учёный предпринял ряд весьма смелых шагов.
Во-первых, многочисленные эксперименты позволили Менделееву сделать вывод, что атомные массы некоторых элементов ранее были вычислены неправильно, и он изменил их в соответствии со своей системой.
Во-вторых, в таблице были оставлены места для новых элементов, открытие которых учёный предсказал, подробно описав их свойства.

Первый вариант Периодической таблицы элементов, составленной Д.И. Менделеевым.
Мировое научное сообщество поначалу скептически отнеслось к открытию русского химика. Однако вскоре были открыты предсказанные им химические элементы: галлий, скандий и германий. Это разрушило сомнения в правильности системы Менделеева, которая навсегда изменила науку. Там, где раньше учёному требовалось провести ряд сложнейших (и даже не всегда возможных в реальности) опытов — теперь стало достаточно одного взгляда в таблицу.
Теперь расскажем, как устроена Периодическая таблица элементов Менделеева и как ею пользоваться.
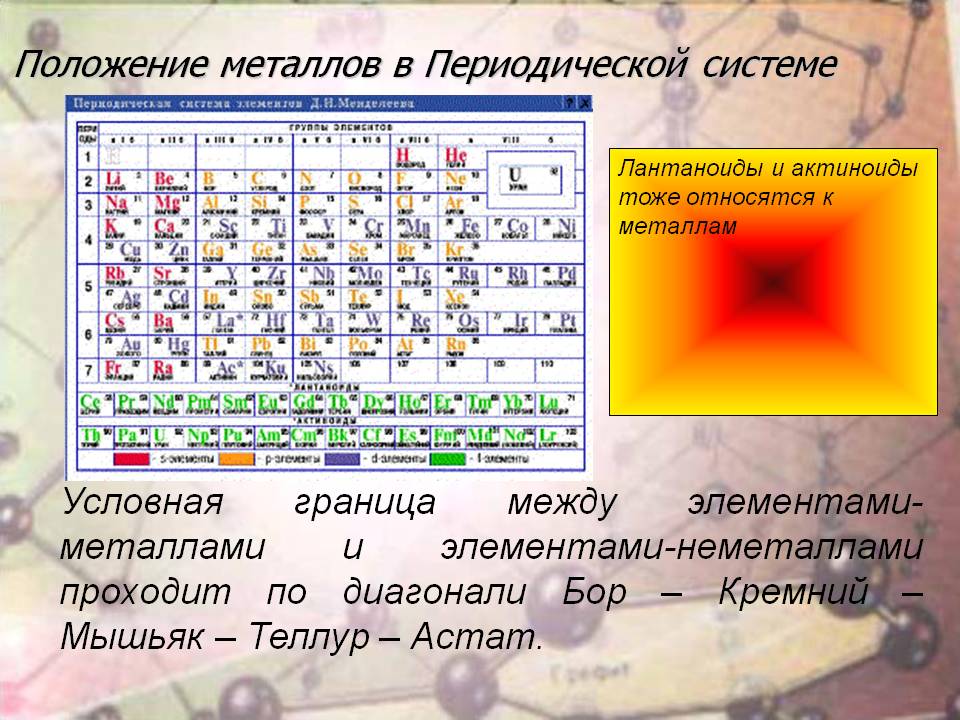
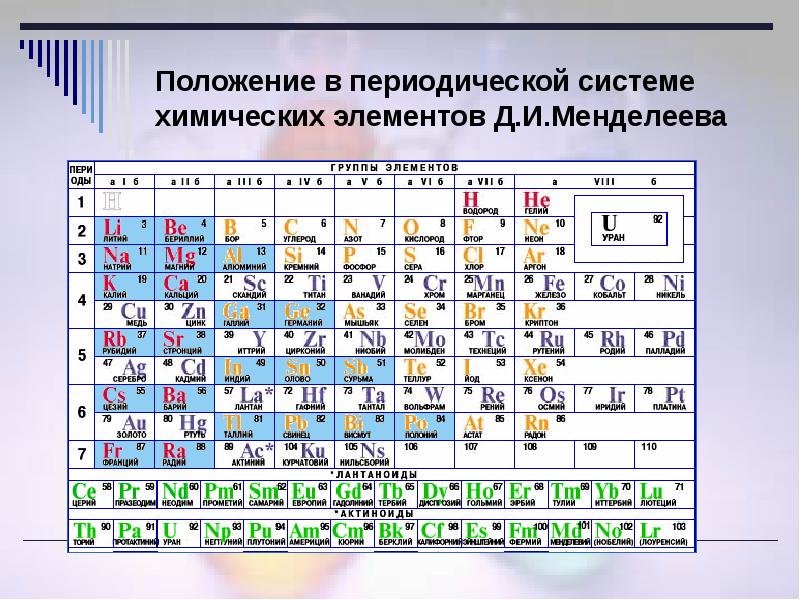
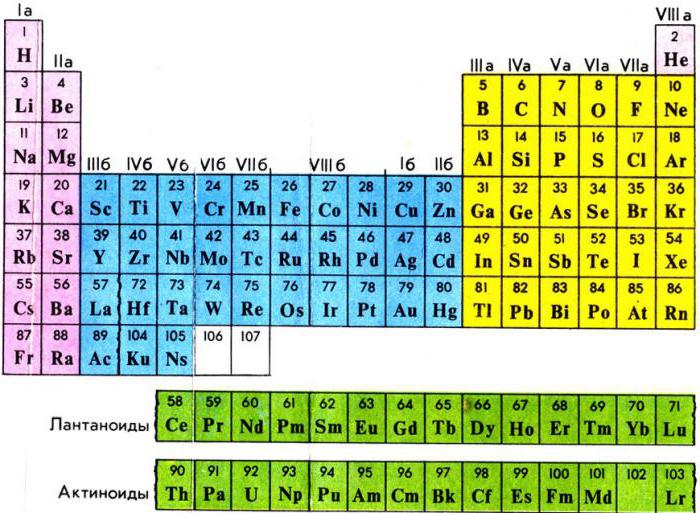
Место внутренних переходных элементов в периодической системе Д. И. Менделеева
В третьей группе шестого – большего периода – за лантаном находится семейство металлов, расположенных от церия и до лютеция включительно. У атома лантана 4f-подуровень пустой, а у лютеция полностью наполнен 14-ю электронами. У элементов, расположенных между ними, идет постепенное заполнение f-орбиталей. В семействе актиноидов – от тория до лоуренсия – соблюдается тот же принцип накопления отрицательно заряженных частиц с единственным отличием: заполнение электронами происходит на 5f-подуровне. Строение же внешнего энергетического уровня и количество отрицательных частиц на нем (равное двум) у всех вышеперечисленных металлов одинаково. Данный факт отвечает на вопрос о том, почему лантаноиды и актиноиды, названные внутренними переходными элементами, имеют много черт сходства.
В некоторых источниках химической литературы представителей обоих семейств объединяют во вторые побочные подгруппы. В них содержится по два металла из каждого семейства. В короткой форме периодической системы химических элементов Д.И Менделеева представители этих семейств выделены из самой таблицы и расположены отдельными рядами. Поэтому положение лантаноидов и актиноидов в периодической системе отвечает общему плану строения атомов и периодичности заполнения электронами внутренних уровней, а присутствие одинаковых степеней окисления послужило причиной объединения внутренних переходных металлов в общие группы. В них химические элементы обладают признаками и свойствами, равнозначными лантану или актинию. Вот почему лантаноиды и актиноиды вынесены из таблицы химических элементов.
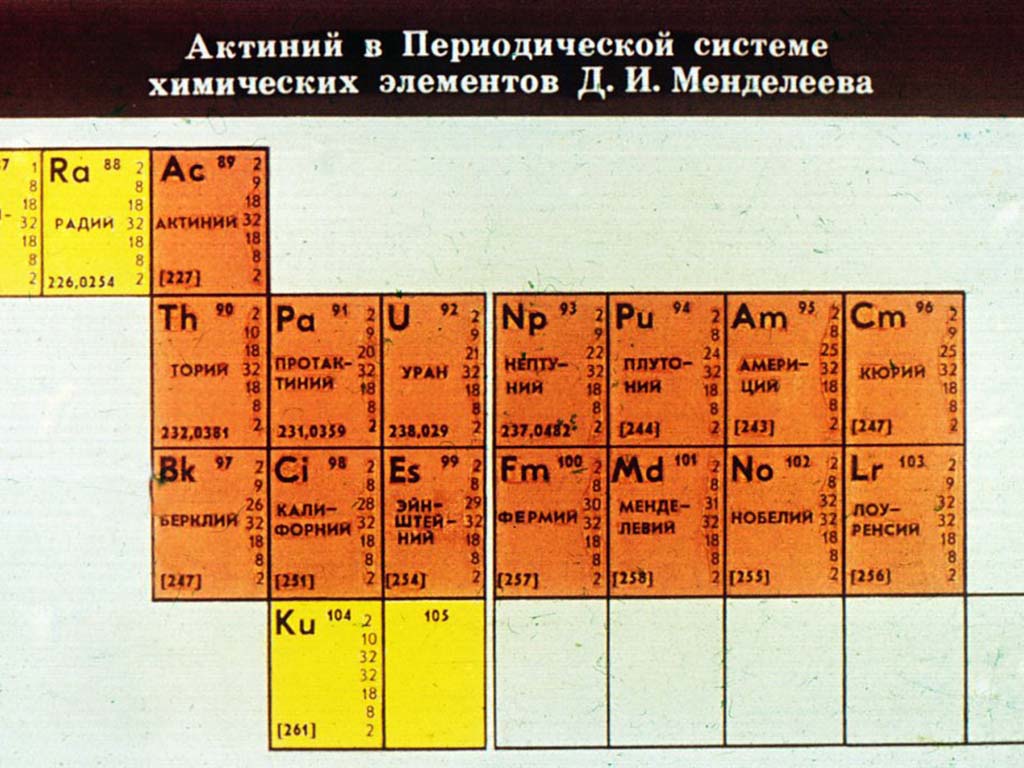
Общие способы получения металлов в промышленности
За исключением тория, протактиния и урана, которые добывают прямым путем из руд, остальные актиноиды можно получить путем облучения образцов металлического урана быстродвижущимися потоками нейтронов. В промышленных масштабах нептуний и плутоний добывают из отработанного топлива ядерных реакторов. Отметим, что получение актиноидов – это достаточно сложный и дорогостоящий процесс, основными методами которого являются ионный обмен и многостадийная экстракция. Лантаноиды, которые называют редкоземельными элементами, получают путем электролиза их хлоридов или фторидов. Чтобы добыть сверхчистые лантаноиды, используют металлотермический метод.

Распространение в природе
Оксиды актиноидов и лантаноидов часто называют циркониевой, ториевой, иттриевой землями. Они являются основным источником для получения соответствующих металлов. Уран, как главный представитель актиноидов, находится в наружном слое литосферы в форме четырёх видов руд или минералов. Прежде всего, это урановая смолка, представляющая собой двуокись урана. В ней содержание металла самое высокое. Часто диоксиду урана сопутствуют радиевые месторождения (жилы). Они встречаются в Канаде, Франции, Заире. Комплексы ториевой и урановой руды часто содержат руды других ценных металлов, например золота или серебра.

Запасами такого сырья богаты Россия, Южно-Африканская республика, Канада и Австралия. В некоторых осадочных породах содержится минерал карнотит. В его состав, кроме урана, входит еще и ванадий. Четвертый вид уранового сырья – это фосфатные руды и железоурановые сланцы. Их запасы находятся в Марокко, Швеции и США. В настоящее время перспективными считаются также залежи лигнитов и каменного угля, содержащие примеси урана. Их добывают в Испании, Чехии, а также в двух американских штатах – Северной и Южной Дакоте.
– Источник
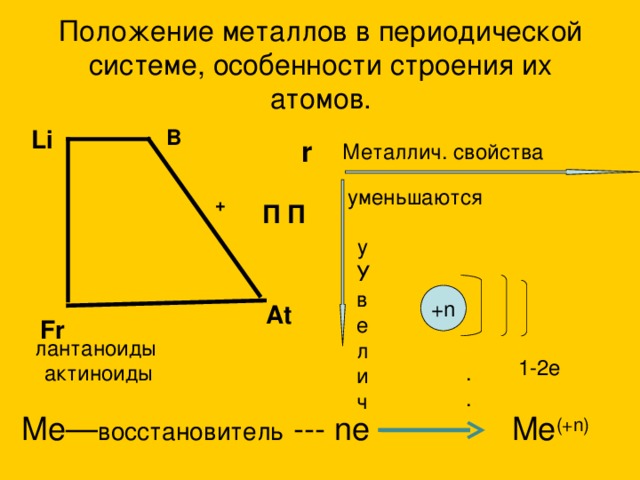
Металлические свойства
Все представители обеих групп являются металлами, у которых достраиваются 4f-, 5f-, а также d-подуровни. Лантан и элементы его семейства называют редкоземельными. Их физические и химические характеристики настолько близки, что по отдельности в лабораторных условиях они разделяются с большим трудом. Проявляя чаще всего степень окисления +3, элементы ряда лантана имеют много сходных черт со щелочноземельными металлами (барием, кальцием, стронцием). Актиноиды также являются чрезвычайно активными металлами, к тому же еще и радиоактивными.
Особенности строения лантаноидов и актиноидов касаются и таких свойств, как, например, пирофорность в мелкодисперсном состоянии. Наблюдается также уменьшение размеров гранецентрированных кристаллических решеток металлов. Добавим, что все химические элементы обоих семейств – это металлы с серебристым блеском, из-за высокой реакционной способности быстро темнеющие на воздухе. Они покрываются пленкой соответствующего оксида, защищающей от дальнейшего окисления. Все элементы достаточно тугоплавки, за исключением нептуния и плутония, температура плавления которых значительно ниже 1000 °С.
Применение лантаноидов
Эти металлы получили достаточно широкое применение. Они используются в качестве добавок при изготовлении различных марок стали, чугуна или других сплавов. Добавление лантаноидов позволяет повысить механическую стойкость, значительно улучшить показатели антикоррозийной устойчивости, улучшить показатели жаропрочности. Особое место они занимают в производстве специальных сортов стекла, которое применяется в атомной технике. В результате добавления лантаноидов в лаки и краски повышают уровень защиты поверхности от коррозии. При определённых составах они придают краскам люминесцирующие свойства. В радиоэлектронике эти металлы добавляют в материалы для изготовления катодов и при создании лазерной техники.
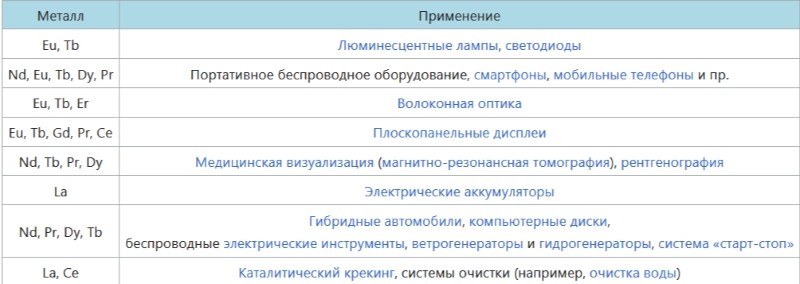
В перспективе планируется применять лантаноиды при создании так называемых оксибромидов, которые будут широко использоваться для проведения ранней диагностики онкологических заболеваний. При приёме этих препаратов кристаллы соединения с лантаноидами будут естественным образом подсвечивать место возникновения раковых клеток.
Использование свойства люминисцентности может быть использовано при создании альтернативных источников освещения, которые могут прийти на смену светодиодам. Разработанные на основе лантаноидов металлогели позволяют находить места появления дефектов в металле, выявление токсинов и патогенов.
Последствия уменьшения ионных радиусов атомов
У лантана и актиния, как и у элементов из их семейств, наблюдается монотонное снижение величины показателей радиусов ионов металлов. В химии в таких случаях принято говорить о лантаноидном и актиноидном сжатии. В химии установлена следующая закономерность: с увеличением заряда ядра атомов, в случае если элементы относятся к одному и тому же периоду, их радиусы уменьшаются. Объяснить это можно следующим образом: у таких металлов, как церий, празеодим, неодим, количество энергетических уровней в их атомах неизменно и равно шести. Однако заряды ядер соответственно увеличиваются на единицу и составляют +58, +59, +60. Это значит, что возрастает сила притяжения электронов внутренних оболочек к положительно заряженному ядру. Как следствие происходит уменьшение радиусов атомов. В ионных соединениях металлов с увеличением порядкового номера ионные радиусы также уменьшаются. Аналогичные изменения наблюдаются и у элементов семейства актиния. Вот почему лантаноиды и актиноиды называют близнецами. Уменьшение радиусов ионов приводит в первую очередь к ослаблению основных свойств гидроксидов Се(ОН)3, Pr(OH)3, а основание лютеция уже проявляет амфотерные свойства.
К неожиданным результатам приводит заполнение 4f-подуровня неспаренными электронами до половины орбиталей у атома европия. У него радиус атома не уменьшается, а, наоборот, увеличивается. У следующего за ним в ряду лантаноидов гадолиния на 5d-подуровне появляется один электрон 4f-подуровня аналогично Eu. Такое строение вызывает скачкообразное уменьшение радиуса атома гадолиния. Подобное явление наблюдается в паре иттербий – лютеций. У первого элемента радиус атома большой по причине полного заполнения 4f-подуровня, а у лютеция он скачкообразно уменьшается, так как на 5d-подуровне наблюдается появление электронов. У актиния и других радиоактивных элементов этого семейства радиусы их атомов и ионов изменяются не монотонно, а, так же как и у лантаноидов, скачкообразно. Таким образом, лантаноиды и актиноиды являются элементами, у которых свойства их соединений коррелятивно зависят от ионного радиуса и строения электронных оболочек атомов.
Химические свойства лантаноидов
Задача 1061. Чем объясняется сходство химических свойств лантаноидов?Решение: К семейству лантаноидов принадлежат четырнадцать f-элементов, следующих в периодической системе после лантана (элементы № 58 – № 71). С возрастанием порядкового номера элементов этого семейства происходит заполнение электронами подуровня третьего снаружи электронного слоя (4f-подуровня), строение же наружного, а у некоторых элементов и следующего за ним слоёв, остаются неизменными. По этой причине все лантаноиды очень близки друг к другу по химическим свойствам. Электроны заполняют 4f-, а не 5-дуровень потому, что в этом случае они обладают меньшей энергией. Однако разница в энергиях 4f- и 5d-состояний очень мала. Благодаря этому один из 4f-элементов (у некоторых, например, у церия, два 4f-электрона) легко возбуждаются, переходя на 5d-подуровень. Поэтому в большинстве своих соединений лантаноиды имеют степень окисления +3, а не +2. Это обстоятельство объясняет близость свойств лантаноидов и скандия. Лантаноиды образуют сульфиды, хлориды, оксиды – солеподобные, нерастворимые, тугоплавкие соединения. Гидроксиды М(ОН)3 – сильные основания. Катионы М3+ сильно гидратируются. С анионами одноосновных кислот и серной кислотой лантаноиды дают растворимые соли. Лантаноиды образуют многочисленные комплексные соединения. Соли их имеют различное яркое окрашивание, что возможно объяснить переходом 4f-электрона на 5d-подуровень.
Лантаноидное сжатие
Задача 1062. Что такое лантаноидное сжатие? Как оно сказывается на свойствах d-элементов 6 периода?Решение: С ростом атомного номера у лантаноидов наблюдается значительное уменьшение металлических и ионных радиусов (от 102 пм у церия Се до 96,1 пм у лютеция Lu). Это явление называется лантаноидным сжатием. Оно является причиной значительного роста плотности лантаноидов: от 6,19 у лантана La до 9,87 у лютеция Lu.
Основная причина лантаноидного сжатия заключается в недостаточном экранировании заряда ядра электронами 4f-орбитали.
В атомах, обладающих единственным электроном, среднее расстояние между ядром и электроном определяется электронной орбиталью, на которой находится электрон, и уменьшается с ростом заряда ядра, тем самым приводя к уменьшению величины атомного радиуса. атомах, обладающих более чем одним электроном, степень уменьшения атомного радиуса вследствие увеличения заряда ядра ослабляется вследствие увеличения электростатического отталкивания между электронами.
характеристики
Кристаллическая структура лантаноидов, кроме церия, самария, европия и иттербия.
Физические свойства
Лантаноиды – это блестящие, серебристые, относительно мягкие и химически активные металлы. Практически все они имеют наиболее плотную упаковку сфер , характерную для металлов . Твердость увеличивается с увеличением атомного номера.
Подобно актинидам , лантаноиды принадлежат к внутренним переходным элементам или элементам f-блока , поскольку f-орбитали в этих рядах не полностью заполнены электронами.
Все изотопы прометия нестабильны, то есть радиоактивны.
Химические свойства
Из-за схожей структуры валентной оболочки лантаноиды химически ведут себя как элементы 3-й группы скандия и иттрия периодической таблицы и вместе с ними образуют группу редкоземельных элементов . На воздухе они быстро окисляются и тускнеют. Они более или менее быстро реагируют с водой с образованием водорода .
Начиная с Cer, постепенно заполняется орбиталь 4f. В случае лютеция он полностью занят 14 электронами. Поскольку 4f-орбитали лежат глубоко внутри атомов , они мало влияют на химическое поведение в отличие от d-орбиталей других элементов подгруппы. Таким образом, элементы лантаноидов относительно схожи по своим химическим свойствам. Они настолько похожи, что когда в 1794 году была открыта эта земля, их даже считали оксидом одного и того же элемента. То же самое относится и к многочисленным компонентам церитовой земли. Их объединяет степень окисления +3. Кроме того, у некоторых элементов встречаются степени окисления +2 и +4.
Нарушение непрерывности ионных радиусов между гадолинием и тербием называется разрывом гадолиния в лантаноидах. Это объясняет, почему, несмотря на схожесть лантаноидов, химическое поведение элементов меняется после гадолиния. На химическое поведение можно легко повлиять на разрыв гадолиния. Следа америция достаточно, чтобы комплекс тербия приобрел структурный тип более легких лантаноидов.
Цвета ионов лантаноидов в водном растворе
| Число окисления | 57 год | 58 | 59 | 60 | 61 | 62 | 63 | 64 | 65 | 66 | 67 | 68 | 69 | 70 | 71 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| +2 | Sm 2+ кроваво-красный | Eu 2+ бесцветный | Тм 2+ пурпурно-красный | Yb 2+ желто-зеленый | |||||||||||
| +3 | La 3+ бесцветный | Ce 3+ бесцветный | Пр 3+ желто-зеленый | Nd 3+ фиолетовый | PM 3+ фиолетовый розовый | Sm 3+ темно-желтый | Eu 3+ бесцветный | Gd 3+ бесцветный | TB 3+ бесцветный | Dy 3+ желто-зеленый | Ho 3+ желтый | He 3+ темно-розовый | TM 3+ бледно-зеленый | Yb 3+ бесцветный | Лю 3+ бесцветный |
| +4 | Ce 4+ оранжево-желтый | Пр 4+ желтый | Nd 4+ сине-фиолетовый | TB 4+ красно-коричневый | Dy 4+ оранжево-желтый |
Применение лантана:
- 1. Водород
- 2. Гелий
- 3. Литий
- 4. Бериллий
- 5. Бор
- 6. Углерод
- 7. Азот
- 8. Кислород
- 9. Фтор
- 10. Неон
- 11. Натрий
- 12. Магний
- 13. Алюминий
- 14. Кремний
- 15. Фосфор
- 16. Сера
- 17. Хлор
- 18. Аргон
- 19. Калий
- 20. Кальций
- 21. Скандий
- 22. Титан
- 23. Ванадий
- 24. Хром
- 25. Марганец
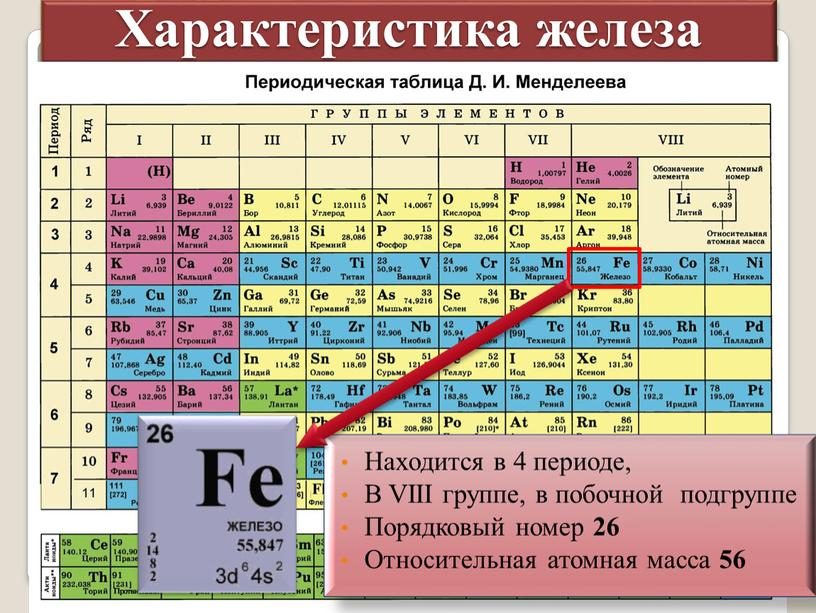
- 26. Железо
- 27. Кобальт
- 28. Никель
- 29. Медь
- 30. Цинк
- 31. Галлий
- 32. Германий
- 33. Мышьяк
- 34. Селен
- 35. Бром
- 36. Криптон
- 37. Рубидий
- 38. Стронций
- 39. Иттрий
- 40. Цирконий
- 41. Ниобий
- 42. Молибден
- 43. Технеций
- 44. Рутений
- 45. Родий
- 46. Палладий
- 47. Серебро
- 48. Кадмий
- 49. Индий
- 50. Олово
- 51. Сурьма
- 52. Теллур
- 53. Йод
- 54. Ксенон
- 55. Цезий
- 56. Барий
- 57. Лантан
- 58. Церий
- 59. Празеодим
- 60. Неодим
- 61. Прометий
- 62. Самарий
- 63. Европий
- 64. Гадолиний
- 65. Тербий
- 66. Диспрозий
- 67. Гольмий
- 68. Эрбий
- 69. Тулий
- 70. Иттербий
- 71. Лютеций
- 72. Гафний
- 73. Тантал
- 74. Вольфрам
- 75. Рений
- 76. Осмий
- 77. Иридий
- 78. Платина
- 79. Золото
- 80. Ртуть
- 81. Таллий
- 82. Свинец
- 83. Висмут
- 84. Полоний
- 85. Астат
- 86. Радон
- 87. Франций
- 88. Радий
- 89. Актиний
- 90. Торий
- 91. Протактиний
- 92. Уран
- 93. Нептуний
- 94. Плутоний
- 95. Америций
- 96. Кюрий
- 97. Берклий
- 98. Калифорний
- 99. Эйнштейний
- 100. Фермий
- 101. Менделеевий
- 102. Нобелий
- 103. Лоуренсий
- 104. Резерфордий
- 105. Дубний
- 106. Сиборгий
- 107. Борий
- 108. Хассий
- 109. Мейтнерий
- 110. Дармштадтий
- 111. Рентгений
- 112. Коперниций
- 113. Нихоний
- 114. Флеровий
- 115. Московий
- 116. Ливерморий
- 117. Теннессин
- 118. Оганесон
- https://en.wikipedia.org/wiki/Lanthanum
- https://de.wikipedia.org/wiki/Lanthan
- https://ru.wikipedia.org/wiki/Лантан
- http://chemister.ru/Database/properties.php?dbid=1&id=267
- https://chemicalstudy.ru/lantan-svoystva-atoma-himicheskie-i-fizicheskie-svoystva/
Примечание: Фото https://www.pexels.com, https://pixabay.com
карта сайта
лантан атомная масса степень окисления валентность плотность температура кипения плавления физические химические свойства структура теплопроводность электропроводность кристаллическая решетка атом нарисовать строение число протонов в ядре строение электронных оболочек электронная формула конфигурация схема строения электронной оболочки заряд ядра состав масса орбита уровни модель радиус энергия электрона переход скорость спектр длина волны молекулярная масса объем атома электронные формулы сколько атомов в молекуле лантана сколько электронов в атоме свойства металлические неметаллические термодинамические
Коэффициент востребованности 504
Литература
|
Атом и молекула лантана. Формула лантана. Строение атома лантана:
Лантан (лат. Lanthanum, от др.-греч. λανθάνω – «скрываюсь», «таюсь») – химический элемент периодической системы химических элементов Д. И. Менделеева с обозначением La и атомным номером 57. Расположен в 3-й группе (по старой классификации – побочной подгруппе третьей группы), шестом периоде периодической системы.
Лантан – металл. Относится к редкоземельным элементам, а также к группе переходных металлов и к лантаноидам.
Как простое вещество лантан при нормальных условиях представляет собой мягкий, ковкий, вязкий, блестящий металл серебристо-белого цвета.
Молекула лантана одноатомна.
Химическая формула лантана La.
Электронная конфигурация атома лантана 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 5d1 6s2 или 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f 5s2 5p6 5d1 6s2. Потенциал ионизации (первый электрон) атома лантана равен 538,09 кДж/моль (5,5769(6) эВ).
Строение атома лантана. Атом лантана состоит из положительно заряженного ядра (+57), вокруг которого по шести оболочкам движутся 57 электронов. При этом 55 электронов находятся на внутреннем уровне, а 2 электрона – на внешнем. Поскольку лантан расположен в шестом периоде, оболочек всего шесть. Первая – внутренняя оболочка представлена s-орбиталью. Вторая – внутренняя оболочка представлены s- и р-орбиталями. Третья, четвертая и пятая – внутренние оболочки представлены s-, р- и d-орбиталями. Шестая – внешняя оболочка представлена s-орбиталью. На внутреннем энергетическом уровне атома лантана на 5d-орбитали находится один неспаренный электрон. На внешнем энергетическом уровне атома лантана на 6s-орбитали находятся два спаренных электрона. В свою очередь ядро атома лантана состоит из 57 протонов и 82 нейтронов. Лантан относится к элементам f-семейства.
Радиус атома лантана (вычисленный) составляет: нет данных. Эмпирический радиус атома лантана составляет 195 пм.
Атомная масса атома лантана составляет 138,90547(7) а. е. м.
Лантан вместе с церием и неодимом относится к наиболее распространенным редкоземельным элементам. Содержание лантана в земной коре составляет 0,0034 %, в морской воде и океане – 3,4×10–10 %.
Лантан без лантаноидов
Как ни грустно сознавать, герой нашего рассказа — личность вполне заурядная. Это металл, обыкновенный по внешнему виду (серебристо-белый, покрытый сероватой окисной пленкой) и по физическим свойствам: температура плавления 920, кипения 3469° С; по прочности, твердости, электропроводности и прочим характеристикам металл лантан всегда оказывается в середине таблиц. Обыкновенен лантан и по химическим свойствам. В сухом воздухе он не изменяется — окисная пленка надежно защищает от окисления в массе. Но если воздух влажен (а в обычных земных условиях он влажен почти всегда), металлический лантан постепенно окисляется до гидроокиси. La(OH)3 — основание средней силы, что опять-таки характерно для металла-«середнячка».
церий
Новый элемент, обнаруженный в церите и мозандерите, по предложению Берцелиуса назвали лантаном. Название с намеком: оно происходит от греческого A,av0dveiv — скрываться, забываться. Лантан, содержащийся в церите, успешно скрывался от химиков в течение 36 лет! Долгое время считали, что лантан двухвалентен, что он аналог кальция и других щелочноземельных металлов, а его атомный вес равен 90—94. В правильности этих цифр не сомневались до 1869 г. Менделеев же увидел, что во II группе периодической системы редкоземельным элементам нет места и поставил их в III группу, приписав лантану атомный вес 138—139. Но правомерность такого перемещения еще надо было доказать. Менделеев предпринял исследование теплоемкости лантана. Полученная им величина прямо указывала на то, что этот элемент должен быть трехвалентным… Металлический лантан, разумеется, далеко не чистый, впервые был получен Мозандером при нагревании хлористого лантана с калием. В наше время в промышленных масштабах получают лантан чистотой более 99%. Проследим, как это делается, но прежде познакомимся с главными минералами лантана и первыми стадиями сложнейшего процесса разделения редкоземельных элементов. Уже упоминалось, что в минералах лантан и лантаноиды неизменно сопутствуют друг другу. Есть минералы селективные, в которых доля того или иного редкоземельного элемента больше, чем обычно. Но нет минералов чисто лантановых или чисто цериевых, не говоря уже о других лантаноидах. Примером селективного лантанового минерала может служить давидит, в котором до 8,3% Lа203 и лишь 1,3% окиси церия. Но получают лантан преимущественно из монацита и бастнезита, как, впрочем, и церий, и все остальные элементы цериевой подгруппы. Монацит — тяжелый блестящий минерал, обычно желто-бурый, но иногда и других цветов, поскольку постоянством состава он не отличается. Точнее всего его состав описывает такая странная формула: (РЗЭ)Р04. Она означает, что монацит — фосфат редкоземельных элементов (РЗЭ). Обычно в монаците 50—68% окислов РЗЭ и 22—31,5% Ра05. А еще в нем до 7% двуокиси циркония, 10% (в среднем) двуокиси тория и 0,1—0,3% урана. Эти цифры со всей очевидностью показывают, почему так тесно переплелись пути редкоземельной и атомной промышленности. Смешанный металл редких земель — мишметалл — и смесь их окислов начали применять в конце прошлого века, а в начале нынешнего в связи с ними был /продемонстрирован выдающийся образец международного воровства. Немецкие суда, доставлявшие грузы в Бразилию, собираясь в обратный путь, заполняли трюмы песком с пляжей Атлантического побережья этой страны, причем из определенных мест. Капитаны заявляли, что песок — это просто балласт, необходимый для большей устойчивости судна. В действительности же они, выполняя заказы германских промышленников, крали ценное минеральное сырье — прибрежные пески штата Эспириту-Санту, богатые монацитом… Монацитовые россыпи распространены по берегам рек, озер и морей на всех континентах. В начале века (данные за 1909 г.) 92% мировой добычи редкоземельного сырья, и прежде всего монацита, приходилось на долю Бразилии. Спустя десять лет центр тяжести переместился на тысячи километров к востоку (или к западу, смотря как считать) — в Индию. После 1950 г. в связи с развитием атомной промышленности гегемоном среди капиталистических стран в добыче и переработке редкоземельного сырья стали Соединенные Штаты.
циркона432Кадмий3празеодима
К 1965 г. внешнеторговые организации нашей страны могли предложить покупателям все лантаноиды в виде металлов чистотой выше 99%. Кроме прометия, разумеется, хотя радиоактивные препараты этого элемента — продукты ядерного распада урана — тоже стали вполне доступны. В каталоги «Техснабэкспорта» вошли также около 300 химически чистых и особо чистых соединений лантана и лантаноидов. Это свидетельство высокого уровня развития советской редкоземельной промышленности. Но вернемся к лантану.